Cryptococcus neoformans
Principaux éléments du diagnostic
- Les analyses de laboratoire de routine sont souvent normales.
- Un tiers des patients sont afébriles.
- Le diagnostic définitif est établi par culture fongique, maintenue à 37°C (98,6°F) pendant 6 semaines.
- L'antigène cryptococcique présente une sensibilité de 95 % en cas d'infection du SNC dans le LCR centrifugé.
- L'examen à l'encre de Chine n'est positif que dans 50 % des cas de méningo-encéphalite.
- Les lymphocytes du LCR sont souvent peu nombreux en cas d'infection du SNC, en particulier chez les patients atteints du SIDA.
- Dans le sérum, l'antigène cryptococcique est la méthode de détection la plus sensible.
- Radiographie thoracique variable : multiples zones d'infiltration dans les lobes inférieurs, le plus souvent en cas d'atteinte pulmonaire.
- La détection moléculaire par PCR pourrait bientôt devenir une pratique standard en laboratoire.
Considérations générales
Épidémiologie et écologie
Cryptococcus neoformans existe sous deux variétés distinctes, connues sous les noms de variété neoformans et variété gattii (Tableau 1). Cryptococcus neoformans variété neoformans est présent dans le monde entier et se trouve fréquemment dans les déjections de pigeon accumulées au fil du temps. Les concentrations de ces organismes sont souvent assez élevées dans les vieilles déjections de pigeon trouvées dans les granges, sur les rebords de fenêtre et autour des étages supérieurs des vieux bâtiments. Les pigeons porteurs de l'organisme ne semblent pas être cliniquement atteints, et les déjections humides ou fraîches contiennent rarement C neoformans. C neoformans variété neoformans a également été isolé dans les déjections d'autres oiseaux, y compris les perruches et les canaris.
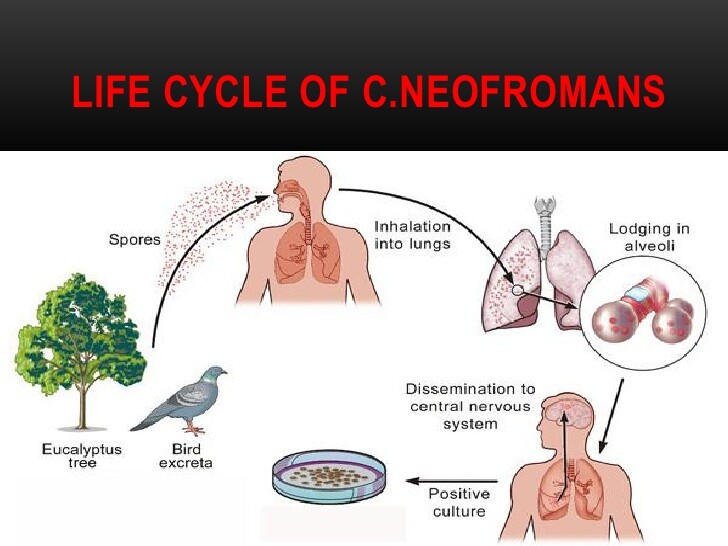
La variété gattii a été isolée le plus fréquemment dans les climats tropicaux et subtropicaux, le plus souvent en Australie, en Asie du Sud-Est, au Brésil, au Venezuela, au Zaïre et dans le sud de la Californie. Cette constatation semble être liée à la répartition de l'eucalyptus à gomme rouge (Eucalyptus camaldulensis), qui héberge l'organisme. L'infectivité est corrélée à la floraison des eucalyptus. L'organisme ne provoque pas d'épidémies ni de clusters d'infection, et l'absence d'antécédent d'exposition aux déjections d'oiseaux ou aux eucalyptus en fleurs ne doit pas exclure le diagnostic d'infection à Cryptococcus - ou de "cryptococcose".
Le SIDA et l'utilisation d'une thérapeutique immunosuppressive ont entraîné une augmentation spectaculaire du nombre d'infections dues à C neoformans au cours des 25 dernières années (voir site). En fait, plus de cas de cryptococcose ont été décrits aux États-Unis en 1976 (338 cas) que n'en avaient été décrits dans le monde en 1955 (~ 300 cas). Avant l'épidémie de SIDA, près de la moitié des cas d'infection à Cryptococcus étaient décrits chez des patients ayant une altération de l'immunité cellulaire, y compris leucémies, lymphomes, sarcoïdose et utilisation chronique de corticostéroïdes, ainsi que chez des patients immunodéprimés ayant subi une transplantation d'organe. Il est intéressant de noter que presque chaque cas de cryptococcose chez des patients atteints du SIDA a été causé par la variété neoformans. Ce phénomène a entraîné une augmentation spectaculaire de l'incidence de cryptococcose causée par la variété neoformans, en particulier en Afrique centrale, où la majorité des infections étaient causées par la variété gattii avant l'épidémie de SIDA. La raison de cette constatation épidémiologique biaisée demeure pour l'instant spéculative.
La cryptococcose demeure l'infection fongique menaçant le plus la vie, et la plus fréquente, chez les patients atteints du SIDA. Elle est généralement observée chez des patients ayant des numérations de CD4 < ; 100 cellules/mm3. Les estimations de la prévalence de la cryptococcose chez les patients atteints du SIDA varient de 6 % à 10 %. C neoformans est également le troisième organisme le plus fréquent affectant le système nerveux central (SNC) dans les cas de SIDA. Il semble exister une variation considérable de la fréquence de la cryptococcose parmi les patients atteints du SIDA dans différentes régions du monde, avec seulement 3 % des patients infectés dans certaines parties de l'Europe mais possiblement ≈ 30 % des Africains subsahariens étant concernés. Les hommes sont atteints environ trois fois plus souvent que les femmes, indépendamment de la présence de SIDA.
Microbiologie
Cryptococcus neoformans est un champignon encapsulé de type levure qui se reproduit par bourgeonnement. Lors du bourgeonnement, une ou deux cellules filles sont souvent observées en cours de libération, mais restent encore reliées à la cellule mère par un fin prolongement de matériel polysaccharidique extracellulaire.
Les cellules de levure encapsulées apparaissent généralement rondes ou ovales dans les échantillons tissulaires et mesurent habituellement 4 à 8 µm. Les cellules de Cryptococcus peuvent atteindre 15 µm lorsqu'elles commencent à bourgeonner. La taille de la capsule polysaccharidique entourant l'organisme varie considérablement et dépend principalement des conditions de croissance environnantes. La taille de la capsule in vitro ne corrèle pas avec la virulence d'une souche particulière.
C neoformans croît à 37°C sur gélose de Sabouraud ou sur gélose au malt, une caractéristique qui distingue cette espèce des autres espèces non pathogènes de Cryptococcus. Les organismes sont généralement visibles dans les 72 heures sous forme de colonies blanches ou beige, mucoïdes et lisses.
La variété neoformans comprend les sérotypes capsulaires A et D, et la variété gattii les sérotypes capsulaires B et C. Les deux variétés de C neoformans peuvent être distinguées sur gélose canavanine-glycol-bleu de bromothymol. La variété gattii croît en produisant un changement de couleur vers un bleu cobalt ; la variété neoformans ne croît pas et l'indicateur reste jaune. De plus, les spp. de Cryptococcus hydrolysent l'urée et assimilent le maltose, le saccharose, le glucose et le galactose, mais pas le lactose. Les glucides ne sont pas fermentés par les espèces de ce genre. C neoformans produit de la mélanine à partir des catécholamines par la phénoloxydase. Cette enzyme a récemment été clonée et caractérisée. Il s'agit d'un type de laccase. La production de mélanine s'est révélée être un facteur de virulence.
Pathogenèse
On pense que C neoformans est acquis par l'homme par inhalation de particules infectées provenant de déjections d'oiseaux (var. neoformans) ou d'arbres d'Eucalyptus camaldulensis en fleurs (var. gattii). Certaines infections causées par C neoformans peuvent résulter de la réactivation d'une infection latente, bien que ce point soit controversé. Il n'existe aucune preuve que l'acquisition se produise directement à partir d'autres humains ou animaux. Le sol contaminé par l'organisme, lorsqu'il est perturbé par le vent, permet à l'organisme de s'aérifier. Les particules inhalées de C neoformans, souvent < ; 2 µm de taille, sont généralement déposées dans les poumons et rapidement phagocytées par les macrophages alvéolaires. Cette réponse cellulaire chez les hôtes normaux aboutit généralement à une infection inapparentée. On ne sait pas si l'organisme est habituellement éradiqué à ce stade, mais des rapports anecdotiques suggèrent qu'un état dormant peut survenir chez certains individus. Lors de l'exposition primaire, un défaut de l'immunité cellulaire ou un inoculum particulièrement important peut conduire à la prolifération et à la dissémination de l'organisme, le plus souvent vers le SNC.
Les principaux facteurs responsables de la virulence comprennent (a) la capsule polysaccharidique environnante, (b) l'enzyme phénoloxydase, (c) la capacité de croître à 37°C, et (d) le type de partenaire alpha. Il a été démontré que la capsule polysaccharidique nuit à la phagocytose par l'hôte et peut gêner la migration des leucocytes. Les cellules phagocytaires peuvent être incapables d'englober des organismes fortement encapsulés en raison de la taille du pathogène. Les éléments capsulaires activent également le système du complément, ce qui a probablement un effet significatif sur la défense de l'hôte, selon la quantité de matériau capsulaire entourant l'organisme. De plus, la voie alternative du complément pourrait être activée par des composants de la paroi cellulaire, ce qui pourrait épuiser localement les facteurs humoraux de l'hôte. Les mécanismes de destruction oxydative des macrophages et des neutrophiles sont des éléments importants de la défense de l'hôte et peuvent être entravés par les spp. de Cryptococcus. C neoformans produit l'enzyme phénoloxydase, qui convertit les substrats hydroxybenzoïques en mélanine. Cette activité peut protéger contre les défenses oxydatives de l'hôte. Il n'a jamais été démontré que l'organisme produisait des toxines.
Avant l'avènement de la thérapie antirétrovirale hautement active (HAART), la cryptococcose entraînait une forte mortalité. Lors du diagnostic et du traitement initial par antifongiques, ≈ 25 % des patients atteints du SIDA sont décédés. Un an après le diagnostic de C neoformans, 30-60 % des patients atteints du SIDA sont décédés de la maladie. Les patients cancéreux diagnostiqués avec une méningite cryptococcique ont une survie médiane globale d'à peine 2 mois. Ces constatations soulignent l'importance de l'immunocompétence dans la susceptibilité à la cryptococcose et sa corrélation avec la gravité, qu'il s'agisse du SIDA ou d'une maladie lymphoréticulaire maligne.
Constatations cliniques
Signes et symptômes
Infection du SNC. La manifestation clinique la plus fréquente de l'infection à C neoformans est l'infection chronique du cerveau et des méninges, appelée méningo-encéphalite. L'utilisation de ce terme est devenue habituelle car les organismes cryptococciques envahissent véritablement le parenchyme cérébral, cérébelleux et du tronc cérébral, ainsi que les méninges.
Le symptôme le plus fréquent de la méningo-encéphalite est la céphalée. Les signes d'inflammation méningée, y compris la raideur de la nuque et la photophobie, sont présents chez ~ 50 % des patients mais sont habituellement légers. Fatigue, vertiges et nausées peuvent également être présents. À mesure que la maladie progresse sur plusieurs semaines, les patients peuvent développer un état mental modifié, une perte visuelle, des paralysies des nerfs crâniens, une ataxie, des convulsions, un coma et une hernie du tronc cérébral. Les signes et symptômes d'une augmentation de la pression intracrânienne peuvent prédominer, y compris céphalées sévères, raideur de la nuque, vomissements en jet, altération de la conscience et papilloème. De nombreux patients atteints de cryptococcose n'ont jamais de fièvre.

Infection pulmonaire
La maladie pulmonaire est une autre manifestation potentiellement fatale de l'infection par C neoformans. Cependant, la majorité des patients présentent probablement une maladie infraclinique, la moitié ne présentant pas de symptômes. Néanmoins, l'étendue de la maladie peut aller d'une pneumonie aiguë et autolimitée chez des individus par ailleurs sains, ou d'une colonisation chronique et stable chez des patients ayant une maladie pulmonaire sous-jacente, à une pneumonie sévère et progressive chez des patients atteints du SIDA, avec une mortalité approchant 50 %. Les symptômes les plus fréquents observés dans l'infection pulmonaire incluent la toux sèche, une fièvre légère, la production de crachats et une douleur thoracique pleurétique. Les épanchements pleuraux sont rarement visibles à la radiographie thoracique. La dissémination au SNC doit probablement être considérée comme la complication la plus grave de la cryptococcose pulmonaire. Elle peut survenir à n'importe quel stade de l'infection pulmonaire, même lorsque l'atteinte pulmonaire semble être en voie de résolution.
Autres infections
C neoformans peut également affecter d'autres systèmes d'organes. Des lésions cutanées peuvent être observées chez ≈ 10 % des patients et signifient une maladie disséminée avec un risque élevé d'atteinte du SNC. Jusqu'à 5-10 % des patients ont une atteinte squelettique par cryptococcose. Les vertèbres et les os longs sont le plus souvent touchés. La cryptococcose peut affecter les yeux, le cortex surrénalien, le système génito-urinaire, le système gastro-intestinal et, dans de rares cas, pratiquement tout autre système d'organe.
Infections chez les patients atteints du SIDA ou immunodéprimés
Chez les patients infectés par le virus de l'immunodéficience humaine (VIH), la cryptococcose est considérée comme une maladie définissant le SIDA. L'évolution clinique de l'infection du SNC chez les patients atteints du SIDA semble être plus aiguë, la fièvre et le mal de tête étant prédominants au début du tableau. Les constats sont similaires à ceux observés chez les patients non SIDA à mesure que la maladie progresse, mais peuvent se développer plus rapidement. La grande majorité des patients atteints du SIDA présentent une méningo-encéphalite au moment du diagnostic de cryptococcose. La maladie pulmonaire semble provoquer des symptômes plus fréquemment chez les patients atteints du SIDA, avec une plus grande proportion présentant fièvre, toux, dyspnée et perte de poids. Les organismes cryptococciques peuvent être cultivés à partir de sites en dehors du SNC chez < ; 20 % des patients atteints du SIDA. Les lésions cutanées sont plus fréquentes chez les patients atteints du SIDA et ressemblent souvent aux papules observées dans l'infection à molluscum contagiosum. L'atteinte du foie et de la rate est probablement plus fréquente chez les patients atteints du SIDA mais reste néanmoins rare.
Résultats de laboratoire
Les analyses de laboratoire de routine, y compris les numérations leucocytaires, l'hématocrite et les bilans sanguins, sont souvent normales dans la cryptococcose, même dans les infections sévères. L'identification moléculaire de C neoformans dans le sérum et d'autres liquides et tissus par réaction en chaîne par polymérase pourrait bientôt devenir une pratique standard dans de nombreux laboratoires.
Infection du SNC
Le diagnostic d'infection du SNC par C neoformans est établi de façon définitive par la culture fongique du culot du LCR centrifugé. Les milieux de culture doivent être maintenus en aérobiose à 37°C pendant 6 semaines avant qu'une culture ne soit considérée comme négative. L'antigène cryptococcique est positif par agglutination au latex dans près de 95 % des cas dans le surnageant du LCR centrifugé. Des dilutions scalaires du LCR réalisées par agglutination au latex permettent de rapporter des titres, ce qui peut être utile pour évaluer le pronostic ou surveiller la réponse au traitement chez les patients non immunodéprimés. Les titres d'antigène ne semblent pas corréler avec la gravité de l'infection ou la réponse au traitement chez les patients atteints du SIDA. La présence d'antigène cryptococcique dans le sérum est évocatrice mais non diagnostique d'une atteinte du SNC chez les patients non SIDA. Cependant, ≈ 95 % des patients atteints du SIDA avec une infection documentée du SNC auront un antigène cryptococcique positif dans le sérum. L'identification positive des organismes cryptococciques dans le LCR par préparation à l'encre de Chine se produit dans ≈ 50 % des cas de méningo-encéphalite. Les lymphocytes dans le LCR sont présents en faible nombre, en particulier chez les patients atteints du SIDA. Une étude sur la méningite cryptococcique chez des patients atteints du SIDA a montré une moyenne de quatre lymphocytes/mm3 dans le LCR. Le glucose du LCR est généralement bas mais peut être normal. La protéine dans le LCR est habituellement élevée, tout comme la pression d'ouverture. La tomodensitométrie et l'imagerie par résonance magnétique peuvent détecter la présence de nodules (cryptococcomes), d'hydrocéphalie ou de rehaussement gyral. Près de 50 % des patients peuvent présenter une tomodensitométrie anormale. Des cryptococcomes peuvent être observés chez ≈ 25 % des patients atteints de méningo-encéphalite.
Infection pulmonaire
Diagnostiquer la présence de C neoformans dans le poumon est moins satisfaisant et plus difficile à interpréter. La colonisation par des organismes cryptococciques a souvent été notée sur des cultures répétées d'expectoration de patients ayant une maladie pulmonaire chronique. La culture d'expectoration ou de lavage broncho-alvéolaire doit être considérée comme le standard de référence pour le diagnostic de cryptococcose pulmonaire. Les patients présentant des symptômes de maladie pulmonaire et des titres d'antigène cryptococcique ≈ 8 sur des prélèvements de lavage broncho-alvéolaire doivent être considérés comme ayant une cryptococcose pulmonaire. La radiographie thoracique peut ne pas être nécessairement utile dans le diagnostic d'une maladie pulmonaire suspectée. Le plus souvent, les radiographies thoraciques sont normales ou montrent un tableau non spécifique d'infiltrats interstitiels et d'adénopathie. Occasionnellement, des patients présentent de multiples nodules volumineux et denses qui s'avèrent par la suite être causés par la cryptococcose. Les épanchements pleuraux sont rarement notés aux radiographies thoraciques.
Le diagnostic d'une infection disséminée dans la circulation sanguine - ou "cryptococcémie" - est mieux établi sur la base de la présence d'antigène cryptococcique, détecté par agglutination au latex ou en cultivant les organismes en utilisant des hémocultures "isolator". Le polysaccharide de la capsule devient soluble dans le sérum des patients infectés et peut être détecté avec un antisérum de lapin anti-C neoformans avec ≈ 95 % de sensibilité. Des titres d'antigène ≈ 8 sont considérés comme signalant une maladie active. Cette méthode de détection de l'infection à C neoformans est plus sensible que la culture ou la coloration à l'encre de Chine, qui sont respectivement d'environ 75 % et 50 % sensibles. Des faux positifs de détection d'antigène peuvent survenir chez des patients ayant un facteur rhumatoïde dans le sang ou par réaction croisée avec l'antigène polysaccharidique de Trichosporon beigelii.
Autres infections
Les lésions cutanées et muqueuses, qui peuvent être secondaires à une cryptococcose disséminée, doivent faire l'objet d'une biopsie à la fois pour le diagnostic histologique et pour la culture. Les lésions squelettiques doivent également être biopsiées si le diagnostic est douteux.
Traitement
Le traitement des patients atteints de cryptococcose est déterminé par le statut VIH (positif ou négatif) et selon qu'ils présentent une atteinte pulmonaire localisée ou disséminée (généralement méningite).
Patients séronégatifs pour le VIH
En cas d'infection pulmonaire légère à modérée sans preuve de dissémination, le fluconazole oral pendant 6-12 mois est adéquat (Tableau 2). En cas de méningite, cryptococcémie ou infection pulmonaire sévère, le traitement préféré comprend une combinaison d'amphotéricine B plus 5-flucytosine pendant 2 semaines, suivie de fluconazole oral par jour pendant un minimum de 10 semaines (Tableau 2). La 5-flucytosine est administrée toutes les 6 h. Les taux sériques doivent être surveillés et la dose ajustée pour obtenir des concentrations maximales de 20-40 µg/ml. Des numérations globulaires complètes sont requises pour détecter la toxicité et doivent être effectuées deux fois par semaine.
L'amphotéricine B est limitée par des effets indésirables et des complications importants, notamment la toxicité liée à la perfusion, la néphrotoxicité et l'hypokaliémie. La 5-flucytosine provoque une myélosuppression, en particulier une thrombocytopénie et une neutropénie, ainsi que des troubles gastro-intestinaux.
Patients séropositifs pour le VIH
Pour une infection pulmonaire légère à modérée, le fluconazole quotidien à vie est recommandé (Tableau 3). Alternativement, une combinaison de fluconazole plus 5-flucytosine peut être administrée pendant 10 semaines.
Le traitement du SNC avec atteinte pulmonaire sévère ou dissémination à d'autres sites corporels comporte deux phases. D'abord, une thérapie d'induction/consolidation est administrée pour contrôler l'infection et réduire le nombre de Cryptococcus viables dans le LCR et les tissus à un niveau indétectable. Cela est suivi par une thérapie d'entretien, qui prévient la rechute. Il n'est actuellement pas clair si la thérapie d'entretien peut être interrompue chez les patients bénéficiant d'une HAART réussie et prolongée. L'induction/consolidation se fait par amphotéricine B plus 5-flucytosine pendant 2 semaines, suivie de fluconazole pendant 10 semaines. La thérapie d'entretien consiste en fluconazole par jour à vie (Tableau 3).
Les interactions médicamenteuses constituent un point important lorsque des antifongiques azolés sont utilisés. Dans un cas, un médicament coadministré (par ex., oméprazole) peut diminuer l'absorption gastro-intestinale (par ex., de l'itraconazole) ou augmenter le métabolisme (par ex., du fluconazole par la rifampine), rendant la thérapie antifongique moins active. À l'inverse, les azolés peuvent entraîner une toxicité inattendue du médicament coadministré (par ex., warfarine) en modifiant le métabolisme hépatique via le système cytochrome P-450. Les interactions médicamenteuses chez les patients infectés par le VIH prenant des schémas thérapeutiques complexes nécessitent un examen attentif au moment d'initier une thérapie antifongique, en particulier un azolé.
Une autre considération importante dans le traitement de la méningite cryptococcique est l'hypertension intracrânienne. Une grande proportion des décès, en particulier en début d'évolution, est attribuable à une hypertension intracrânienne. Les patients qui se présentent avec, ou qui développent, un coma ou d'autres signes d'augmentation de la pression intracrânienne devraient subir une ponction lombaire quotidienne avec retrait de 30 cc de LCR, jusqu'à résolution des symptômes. Un traitement par acétazolamide et la dérivation ventriculopéritonéale ont également été essayés. L'effet de ces interventions sur la mortalité est inconnu.
Pronostic
La guérison de la cryptococcose du SNC chez les patients atteints du SIDA est rare. Par conséquent, la prise en charge vise une thérapie de suppression à long terme. L'effet de la HAART sur la capacité à guérir la cryptococcose est inconnu. Un suivi rapproché tout au long du traitement initial et du traitement d'entretien est impératif dans la cryptococcose associée au SIDA pour surveiller la rechute. Les patients immunodéprimés atteints d'une maladie néoplasique peuvent également être difficiles à guérir et nécessiter une thérapie suppressive à long terme. Chez d'autres, le taux de mortalité des infections du SNC traitées peut être de 25-30 %, bien que cela varie selon les séries. Souvent, le pronostic est largement influencé par l'état d'immunosuppression sous-jacent, par exemple, dans les maladies lymphoréticulaires malignes.
Les facteurs indiquant un mauvais pronostic comprennent un état mental anormal, un âge avancé (> ; 60 ans), la cryptococcémie, des titres élevés d'antigène cryptococcique dans le LCR ou le sang, et des mesures du LCR montrant une pression d'ouverture élevée, un faible nombre de globules blancs (< ; 20 cellules/mm3), un faible glucose, et une préparation à l'encre de Chine positive. Les complications morbides graves incluent le syndrome cérébral chronique avec démence et l'hydrocéphalie aiguë et chronique.
Prévention et contrôle
La prophylaxie contre la cryptococcose n'est pas actuellement recommandée. Cependant, chez les patients atteints du SIDA avec des numérations de CD4 < ; 200 cellules/mm3, l'incidence de la cryptococcose a été réduite de 7 % à 1 % chez les patients prenant du fluconazole (200 mg PO par jour). Il peut être approprié de faire éviter aux patients atteints du SIDA, ou à d'autres patients immunodéprimés, les zones fortement peuplées de pigeons. L'utilisation d'une immunisation active avec le polysaccharide capsulaire n'a pas été concluante.
| Caractéristique | Variété neoformans | Variété gattii |
|---|---|---|
| Répartition géographique | Dans le monde entier | Régions tropicales et subtropicales |
| Réservoir | Déjections de pigeon | Arbres d'eucalyptus |
| Prédisposition de l'hôte | SIDA, sarcoïdose, lymphome, corticostéroïdes, LLC, LLA, transplantation d'organe | Principalement hôtes normaux |
| Infection chez les patients SIDA | Oui | Rare |
| Scénario clinique | Choix | Schéma |
|---|---|---|
| Maladie pulmonaire légère à modérée | Premier choix | Fluconazole, 200-400 mg/jour pendant 6-12 mois |
| Maladie pulmonaire légère à modérée | Deuxième choix | Amphotéricine B, 0,5-1,0 mg/kg/jour (total, ~ 1000-2000 mg) |
| SNC ou maladie pulmonaire sévère | Premier choix | Amphotéricine B, 0,7-1,0 mg/kg/jour pendant 2 semaines ; puis fluconazole, 400 mg/jour pour un minimum de 10 semaines |
| SNC ou maladie pulmonaire sévère | Deuxième choix | Amphotéricine B, 0,7-1,0 mg/kg/jour plus 5-flucytosine, 100 mg/kg/jour pendant 6-10 semaines |
| Scénario clinique | Phase/choix | Schéma |
|---|---|---|
| Maladie pulmonaire légère à modérée | Premier choix | Fluconazole, 200-400 mg/jour (à vie) |
| Maladie pulmonaire légère à modérée | Deuxième choix | Fluconazole, 400 mg/jour plus flucytosine, 100 mg/kg/jour pendant 10 semaines |
| SNC, atteinte pulmonaire sévère ou dissémination à d'autres sites | Induction/consolidation (premier choix) | Amphotéricine B, 0,7-1,0 mg/kg/jour plus 5-flucytosine, 100 mg/kg/jour pendant 2 semaines ; puis fluconazole, 400 mg/jour pour un minimum de 10 semaines |
| SNC, atteinte pulmonaire sévère ou dissémination à d'autres sites | Entretien (premier choix) | Fluconazole, 200-400 mg PO par jour à vie |
| SNC, atteinte pulmonaire sévère ou dissémination à d'autres sites | Induction/consolidation (deuxième choix) | Amphotéricine B, 0,7-1,0 mg/kg/jour pendant 6-10 semaines |
| SNC, atteinte pulmonaire sévère ou dissémination à d'autres sites | Entretien (deuxième choix) | Itraconazole, 200 mg PO deux fois par jour à vie |
En savoir plus
https://en.wikipedia.org/wiki/Cryptococcus_neoformans
https://www.cdc.gov/fungal/diseases/cryptococcosis-neoformans/index.html
https://microbewiki.kenyon.edu/index.php/Cryptococcus_neoformans

















