Toxoplasma gondii
Considérations générales
Épidémiologie
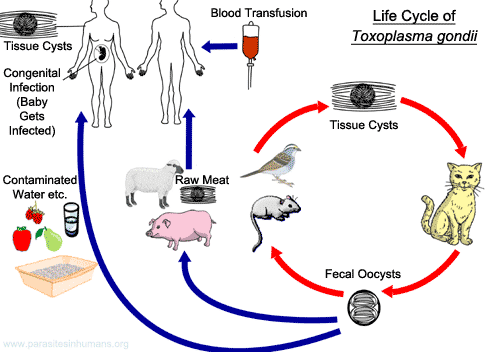
L'infection par Toxoplasma gondii, ou toxoplasmose, est une zoonose (les hôtes définitifs sont des membres de la famille des chats). Les deux voies d'infection les plus courantes chez l'homme sont l'ingestion orale du parasite et la transmission transplacentaire (congénitale) au fœtus. L'ingestion de viande insuffisamment cuite ou crue contenant des kystes, ou d'eau ou d'aliments contaminés par des oocystes, entraîne une infection aiguë.
Chez l'homme, la prévalence de la toxoplasmose augmente avec l'âge. Il existe également d'importantes différences géographiques des taux de prévalence (par ex. : 10 % à Palo Alto, CA ; 15 % à Boston, MA ; 30 % à Birmingham, AL ; 70 % en France ; environ 90 % au Salvador). Les différences dans l'épidémiologie de l'infection à T. gondii selon les régions géographiques et entre groupes de population au sein d'une même région peuvent s'expliquer par des différences d'exposition à l'organisme. Occasionnellement, des foyers surviennent au sein de familles ou de certaines populations. La possibilité d'un foyer doit toujours être envisagée pour chaque cas d'infection aiguë récemment acquise.

L'incidence de la toxoplasmose congénitale est directement corrélée à trois facteurs : (1) la prévalence de l'infection primaire chez les femmes pendant la grossesse, (2) l'âge gestationnel auquel la femme enceinte acquiert l'infection, et (3) le type de programmes de santé publique disponibles pour la prévention, la détection et le traitement de l'infection pendant la grossesse. Bien que le dépistage de l'infection à Toxoplasma soit obligatoire pendant la grossesse dans certains pays tels que l'Autriche et la France, le dépistage sérologique systématique n'est pas pratiqué aux États-Unis. Sans intervention thérapeutique, l'incidence de la toxoplasmose congénitale est d'environ 15 % pour un fœtus dont la mère est infectée au cours du premier trimestre, 30 % au cours du deuxième trimestre et 60 % au cours du troisième trimestre. La spiramycine diminue l'incidence de l'infection fœtale d'environ 60 %. Il a été rapporté que, si l'infection maternelle est acquise pendant les 2 premières semaines de gestation et que la spiramycine est administrée pendant toute la grossesse, l'incidence de l'infection fœtale est négligeable.
En tant qu'agent opportuniste chez les personnes infectées par le VIH, T. gondii a eu un impact majeur sur la santé publique. L'incidence de la toxoplasmose dans une population infectée par le VIH est directement corrélée à quatre facteurs : (1) la prévalence des anticorps anti-Toxoplasma, (2) le degré d'immunodépression estimé par le taux de CD4, (3) la fréquence d'utilisation de schémas prophylactiques efficaces contre la réactivation de Toxoplasma, et (4) la fréquence d'utilisation d'une thérapie antirétrovirale hautement active. Parmi les individus séropositifs à la fois pour le VIH et Toxoplasma avec des taux de CD4 inférieurs à 100 cellules/mm3, 30 %-50 % développeront une encéphalite toxoplasmique (ET) si une prophylaxie n'est pas utilisée. Des facteurs génétiques peuvent également jouer un rôle dans la prédisposition des patients atteints du sida à cette maladie, sur la base de constatations issues d'un modèle murin d'ET et de l'observation que tous les patients infectés par le VIH avec une sérologie positive pour T. gondii ne développent pas d'ET. L'antigène lymphocytaire humain DQ3 semble être un marqueur génétique de susceptibilité au développement de l'ET chez les patients atteints du sida, et DQ1 pourrait être un marqueur de résistance.
Même avant l'apparition du sida, l'ET avait été reconnue comme une cause majeure de morbidité et de mortalité chez les patients non infectés par le VIH mais immunodéprimés, en particulier chez ceux dont la maladie sous-jacente ou le traitement entraînait un déficit de l'immunité à médiation cellulaire (par ex. : maladie de Hodgkin et transplantation cardiaque, pulmonaire, rénale et de moelle osseuse).
Microbiologie
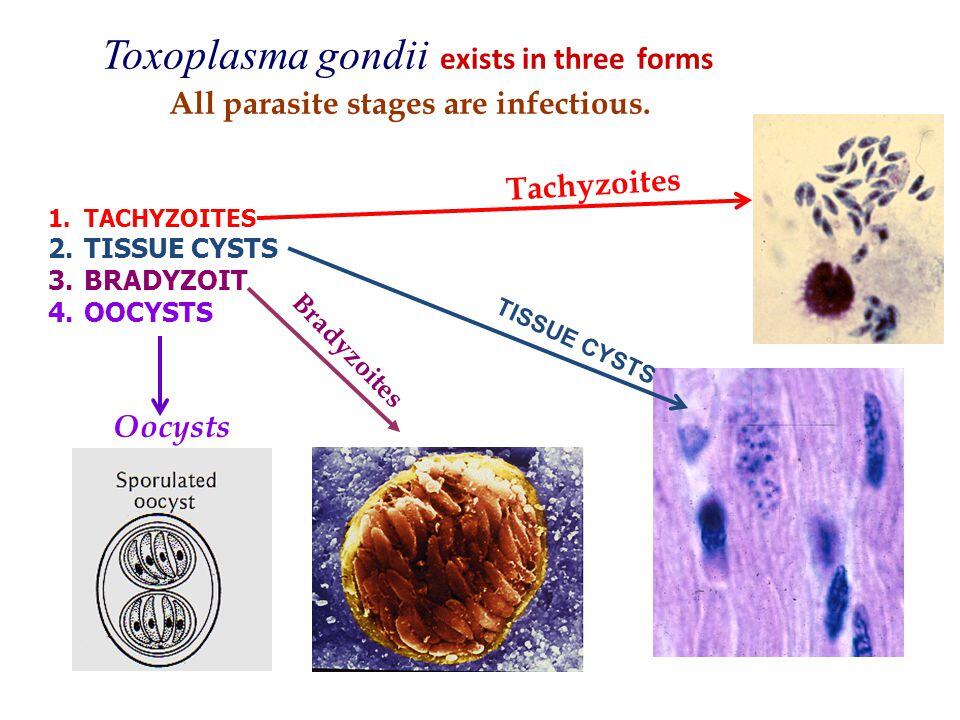
T. gondii est un protozoaire coccidien intracellulaire obligatoire qui existe sous trois formes : l'oocyste (qui libère des sporozoïtes), le tachyzoïte et le kyste tissulaire (qui contient et peut libérer des bradyzoïtes). Le parasite suit deux cycles : un cycle sexué entéroépithélial dans l'intestin grêle des membres de la famille des chats, et un cycle asexué extra-intestinal chez les chats ainsi que chez tous les autres animaux infectés, y compris les humains. Les chats excrètent des oocystes après avoir ingéré l'une des trois formes du parasite. Les humains sont généralement infectés par l'ingestion de kystes tissulaires (dans la viande) ou d'oocystes (dans les fèces de chat) ; les parois externes des deux sont détruites par dégradation enzymatique et les parasites sont libérés dans la lumière intestinale. Ils se transforment en tachyzoïtes et se propagent à pratiquement toutes les cellules et tous les tissus de l'organisme.
- Oocyste. Les oocystes se forment dans l'intestin grêle des membres de la famille des chats et sont excrétés dans leurs fèces pendant 7 à 20 jours. Ils sont très résistants aux conditions de l'environnement externe. Jusqu'à 10 millions d'oocystes peuvent être éliminés en une seule journée et deviennent infectieux (par sporulation) en 1 à 21 jours, selon la température et la disponibilité en oxygène.
- Tachyzoïte. Les tachyzoïtes ont une forme de croissant ou ovoïde et mesurent 2-4 µ ;m de large sur 4-8 µ ;m de long. Ils nécessitent un habitat intracellulaire pour survivre et se multiplier, bien qu'ils possèdent leur propre appareil de Golgi, des ribosomes et des mitochondries. Les tachyzoïtes pénètrent dans les cellules hôtes par un processus actif impliquant les composants d'un " complexe apical " (d'où le terme Apicomplexa). Ils résident et se multiplient dans une vacuole parasitophore intracellulaire dont la composition (par ex. : l'acidité) est dictée en grande partie par le parasite. En laboratoire, les tachyzoïtes sont propagés dans le péritoine de souris et dans des cellules de mammifères en culture tissulaire. La présence de tachyzoïtes dans des liquides ou des tissus humains est le marqueur d'une infection aiguë.
- Kyste tissulaire. Après l'entrée et la réplication de la forme tachyzoïte, une encystation et la formation de kystes tissulaires peuvent se produire. Les conditions précises favorisant la formation de kystes ne sont pas connues. Le kyste tissulaire se forme à l'intérieur d'une cellule hôte et peut varier en taille, depuis des kystes contenant seulement quelques organismes (bradyzoïtes) jusqu'à des kystes d'environ 200 µ ;m de diamètre contenant plusieurs milliers de bradyzoïtes. Les kystes tissulaires se colorent bien avec le réactif périodique acide-Schiff, les colorations de Wright-Giemsa, la méthode de Gomori-méthénamine-argent et les colorations par immunoperoxydase. Les kystes sont sphériques lorsqu'ils se trouvent dans le cerveau et épousent la forme des fibres musculaires lorsqu'ils sont présents dans le muscle cardiaque et squelettique. Les sites les plus courants d'infection latente sont le système nerveux central (SNC), l'œil, ainsi que les muscles squelettiques, lisses et cardiaques. En raison de cette persistance tissulaire, la mise en évidence de kystes dans des coupes histologiques ne signifie pas nécessairement que l'infection a été récemment acquise ni qu'elle est cliniquement pertinente.
- Conversion de stades. Les tachyzoïtes et les bradyzoïtes diffèrent sur le plan phénotypique. Les tachyzoïtes se multiplient rapidement et de manière synchrone, formant des rosaces et lysant ainsi la cellule, tandis que les bradyzoïtes, qui se répliquent plus lentement, forment des kystes tissulaires. D'importantes différences du métabolisme énergétique et de la structure antigénique entre tachyzoïtes et bradyzoïtes reflètent l'expression de voies et de molécules spécifiques à chaque stade, favorisant la survie du parasite dans des environnements divers et dans des conditions variées au sein de l'hôte.
Pathogenèse
T. gondii se multiplie à l'intérieur des cellules au site d'invasion (le tractus gastro-intestinal semble être la principale voie et le site initial d'infection dans la nature). Après la destruction des cellules hôtes, les parasites envahissent les cellules adjacentes, à partir desquelles ils se propagent dans tout le corps via les vaisseaux lymphatiques et la circulation sanguine. L'immunité humorale et l'immunité cellulaire semblent limiter efficacement la phase parasitémique ; seuls les parasites protégés par un habitat intracellulaire ou au sein de kystes tissulaires survivent. Une réponse immunitaire efficace entraîne également une réduction précoce et significative du nombre de T. gondii dans tous les tissus. Par la suite, les tachyzoïtes sont rarement mis en évidence dans les tissus.
La forme kystique tissulaire est responsable de l'infection résiduelle et persiste principalement dans le cerveau, les muscles squelettiques et cardiaques, ainsi que dans l'œil. Bien que la toxoplasmose chez les individus sévèrement immunodéprimés puisse être due à une infection primaire, elle résulte le plus souvent d'une recrudescence d'une infection latente.
Les modifications histopathologiques de la lymphadénite toxoplasmique sont fréquemment diagnostiques chez les individus immunocompétents. Une triade caractéristique de constatations est observée : hyperplasie folliculaire réactive, amas irréguliers d'histiocytes épithélioïdes envahissant et estompant les bords des centres germinatifs, et distension focale des sinus par des cellules monocytoïdes.
L'atteinte oculaire chez les patients immunocompétents provoque une rétinochoroïdite aiguë caractérisée par une nécrose et une inflammation sévère. L'inflammation granulomateuse de la choroïde est secondaire à la rétinite nécrosante.
L'atteinte du SNC se caractérise par des foyers multiples en expansion de nécrose et des nodules microgliaux. La nécrose constitue la caractéristique la plus marquante de la maladie en raison de l'atteinte vasculaire. La présence de multiples abcès cérébraux est la caractéristique la plus typique de l'ET chez les patients sévèrement immunodéprimés et elle est particulièrement évocatrice chez les patients atteints du sida. À l'autopsie, chez la plupart des patients atteints du sida avec ET, les hémisphères cérébraux sont atteints, avec une prédilection particulière pour les ganglions de la base. La toxoplasmose pulmonaire chez le patient immunodéficient peut se présenter sous la forme d'une pneumonite interstitielle, d'une pneumonite nécrosante, d'une consolidation et/ou d'un épanchement pleural. La choriorétinite chez les patients atteints du sida se caractérise par une panophtalmie segmentaire et des zones de nécrose coagulante associées à des kystes tissulaires et à des tachyzoïtes.
Immunité contre T. gondii
Après la maladie chez l'hôte immunocompétent, l'immunité contre T. gondii est durable à vie. L'immunité cellulaire semble plus importante que l'immunité humorale dans la défense du cerveau. Une interaction bien coordonnée entre lymphocytes T CD4 et CD8 ; cellules tueuses activées par lymphokines, cellules tueuses naturelles et cellules T γδ ; et des cytokines telles que l'interféron-γ, le facteur de nécrose tumorale-α, l'interleukine-1 (IL-1), IL-2, IL-4, IL-6, IL-7, IL-10, IL-12 et IL-15 semble déterminer l'issue de l'interaction parasite-hôte humain. L'oxyde nitrique pourrait jouer un rôle protecteur spécifique aux tissus.
Le diagnostic différentiel de la lymphadénite toxoplasmique inclut le lymphome, la mononucléose infectieuse associée au virus Epstein-Barr, la " mononucléose " à CMV, la maladie des griffes du chat, la sarcoïdose, la tuberculose, la tularémie et le carcinome métastatique. Pour l'encéphalite toxoplasmique, le diagnostic différentiel inclut le lymphome primaire du SNC, la leucoencéphalopathie multifocale progressive associée au virus JC, la ventriculite à CMV, le tuberculome, le cryptococcome et les abcès cérébraux bactériens ou à Nocardia. Aucun des signes décrits chez les nouveau-nés atteints de maladie congénitale n'est pathognomonique de la toxoplasmose, et tous peuvent être mimés par une infection congénitale due à d'autres agents pathogènes, y compris le CMV, Treponema pallidum, le virus de l'herpès simplex et le virus de la rubéole.
Complications
Dans de rares cas, la toxoplasmose provoque une myocardite, une polymyosite, une pneumonite, une hépatite ou une encéphalite chez des individus sains. Les infections maternelles précoces entraînent parfois la mort du fœtus in utero et des avortements spontanés.
Prévention et contrôle
La prévention de l'infection primaire est d'une importance capitale chez les femmes enceintes et les patients immunodéficients séronégatifs (Encadré 6). Les kystes tissulaires présents dans la viande deviennent non infectieux si la viande est chauffée à 66 ° ;C (la viande doit être " bien cuite ", sans trace de rose au centre), si elle est fumée ou salée, ou si elle est congelée à -20 ° ;C (température qui n'est pas atteinte dans la plupart des congélateurs domestiques). Les mains doivent être lavées méticuleusement après la manipulation de viande crue ou de légumes ; les œufs ne doivent pas être consommés crus et le lait non pasteurisé (en particulier le lait de chèvre) doit être évité. Les mouches et les cafards doivent être contrôlés. Les zones contaminées par des fèces de chat doivent être totalement évitées. Des gants jetables doivent être portés lors de l'élimination de la litière des chats (si cette tâche ne peut être évitée), lors du jardinage ou du nettoyage d'un bac à sable d'enfant. Les oocystes sont détruits si le contenant de la litière pour chat est trempé dans de l'eau bouillante pendant environ 5 minutes. Si le bac à litière est nettoyé chaque jour, les oocystes n'auront pas le temps de sporuler.
Il n'existe actuellement aucun vaccin pour la prévention de la toxoplasmose chez l'homme ; la prophylaxie primaire contre la toxoplasmose chez les patients atteints du sida à haut risque de développer une ET s'est avérée efficace. La prophylaxie primaire est recommandée pour les patients séropositifs dont le taux de CD4 est inférieur à 100 cellules/mm3 (certains experts utilisent un seuil inférieur à 200 cellules/mm3), indépendamment de la charge virale VIH. Le triméthoprime-sulfaméthoxazole et la dapsone associée à la pyriméthamine ont été rapportés comme des schémas efficaces pour prévenir le premier épisode d'ET (Encadré 7). La pyriméthamine a été utilisée en post-transplantation pour la prophylaxie primaire chez des receveurs de transplantation cardiaque séronégatifs dont les donneurs sont séropositifs (Encadré 7).
| Test ou modalité |
|---|
| Sérologie (IgG) : utile pour établir si le patient a été exposé à T. gondii.1 Elle peut aussi indiquer si l'infection est aiguë ou chronique.2,3 |
| Histologie (hématoxyline et éosine, immunoperoxydase, Wright-Giemsa et colorations périodique acide-Schiff). La présence de tachyzoïtes est diagnostique d'une infection aiguë. Des kystes isolés n'indiquent pas nécessairement une maladie aiguë ou réactivée. |
| Isolement du parasite à partir de n'importe quel tissu par inoculation chez la souris ou en culture tissulaire : diagnostique.2 |
| Détection par PCR de l'ADN dans le liquide amniotique, le LCR, les liquides oculaires, le lavage bronchoalvéolaire, le sang périphérique et l'urine : diagnostique.2 |
| Études radiographiques : utiles en cas de suspicion de toxoplasmose du SNC chez le fœtus ou le nouveau-né (échographie ou scanner) et chez les patients immunodéprimés (scanner ou IRM). |
| Toxoplasmose oculaire : dans la plupart des cas, le diagnostic est clinique. |
- Les tests sérologiques de confirmation incluent le test de coloration de Sabin-Feldman pour IgG, l'ELISA IgM, l'ELISA IgA, le test d'agglutination différentielle et l'ELISA IgE.
- La consultation d'un laboratoire de référence est fortement recommandée.
- Le diagnostic sérologique peut ne pas être utile chez les sujets immunodéprimés.
| Résultat IgG | Résultat IgM | Interprétation et recommandation |
|---|---|---|
| Négatif | Négatif | Aucune preuve sérologique d'infection par T. gondii |
| Négatif | Équivoque ou positif | Infection aiguë possible ou IgM faussement positive ; envoyer l'échantillon à un laboratoire de référence |
| Équivoque pour IgG dans un test différent | Négatif | Indéterminé ; obtenir un nouvel échantillon pour analyse ou refaire le test |
| Équivoque | Équivoque | Indéterminé ; obtenir un nouvel échantillon pour IgG et IgM |
| Équivoque | Positif | Infection aiguë possible ; envoyer l'échantillon à un laboratoire de référence |
| Positif | Négatif | Infection par T. gondii datant de plus de 6 mois |
| Positif | Équivoque ou positif | Infection aiguë possible ; envoyer l'échantillon à un laboratoire de référence |
Modifié à partir de l'avertissement de santé publique de la US Food and Drug Administration : Limitations of Toxoplasma IgM Commercial Test Kits.
| Groupe de patients | Syndromes cliniques |
|---|---|
| Immunocompétent |
|
| Immunodéprimé |
|
| Enceinte |
|
| Fœtus |
|
| Nouveau-né |
|
- Les syndromes ne sont pas mutuellement exclusifs. Les patients peuvent présenter simultanément ou successivement deux syndromes ou plus (par ex. : un patient par ailleurs immunocompétent peut présenter une lymphadénite et une choriorétinite, ou un nouveau-né peut présenter une hydrocéphalie, des calcifications cérébrales et une thrombocytopénie).
| Syndrome | Enfants | Adultes |
|---|---|---|
| Lymphadénite1 | Pas de traitement | Pas de traitement |
| Choriorétinite (active), myocardite, polymyosite, maladie systémique2 |
|
|
- Un traitement peut être indiqué si les symptômes associés sont sévères ou persistants.
- Le rôle d'autres schémas, incluant des médicaments tels que l'atovaquone, la clarithromycine, l'azithromycine, le triméthoprime/sulfaméthoxazole ou la dapsone, n'a pas été bien établi.
- La clindamycine (300 mg par voie orale toutes les 6 heures pendant un minimum de 3 semaines) est une alternative chez les patients allergiques aux sulfamides.
| Syndrome | Médicament | Posologie |
|---|---|---|
| Infection aiguë acquise pendant la gestation | Spiramycine | 3 g/jour ; doit être poursuivie pendant toute la grossesse même si la PCR du liquide amniotique est négative |
| Résultat PCR du liquide amniotique positif à 18 semaines de gestation ou plus tard | Pyriméthamine PLUS sulfadiazine PLUS acide folinique | Commencer après la 18e semaine de gestation ; utiliser les mêmes doses que pour les patients immunocompétents |
| Médicament | Posologie |
|---|---|
| Pyriméthamine | Dose de charge : 2 mg/kg/jour (maximum, 50 mg) pendant 2 jours, puis 1 mg/kg/jour pendant 2 ou 6 mois ; après 2 ou 6 mois, 1 mg/kg/jour les lundi, mercredi et vendredi |
| Sulfadiazine1 | 50 mg/kg toutes les 12 heures |
| Acide folinique | 5-20 mg trois fois par semaine |
| Corticostéroïdes (si indiqué) | 1 mg/kg/jour en 2 prises |
- La clindamycine est une alternative chez les patients allergiques aux sulfamides.
| Composant du schéma | Enfants | Adultes |
|---|---|---|
| Pyriméthamine | Dose de charge : 2 mg/kg/jour (maximum, 50 mg) pendant 2 jours, puis dose d'entretien : 1 mg/kg/jour (maximum 25 mg) | Dose de charge : 200 mg sur 24 heures, suivie de 50-75 mg/jour |
| Sulfadiazine1 | Dose de charge : 75 mg/kg, puis dose d'entretien : 50 mg/kg toutes les 12 heures (maximum 4 g/jour) | Dose de charge : 2-4 g initialement, suivie de 1-1,5 g quatre fois/jour |
| Acide folinique | 5-20 mg trois fois par semaine | 5-10 mg/jour (jusqu'à 50 mg/jour) |
- La clindamycine (300 mg par voie orale toutes les 6 heures pendant un minimum de 3 semaines) est une alternative chez les patients allergiques aux sulfamides.
| Forme infectieuse | Mesures préventives |
|---|---|
| Kyste tissulaire (viande) |
|
| Oocyste (fèces de chat) |
|
| Groupe de patients | Schéma |
|---|---|
| Patients atteints du sida à haut risque de développer une ET | Triméthoprime/sulfaméthoxazole (soit 160 mg/800 mg soit 80 mg/400 mg/jour) ou dapsone (50 mg/jour) plus pyriméthamine (50 mg/semaine) |
| Patients transplantés cardiaques dont les donneurs sont séropositifs | Pyriméthamine 25 mg par voie orale une fois/jour pendant 6 semaines en post-transplantation |
Plus d'informations :
https://www.ncbi.nlm.nih.gov/books/NBK7752/
https://www.cdc.gov/parasites/toxoplasmosis/gen_info/faqs.html

















