Diflucan (Fluconazole)

Posologies
Diflucan 50 mg
| Quantité | Prix par comprimé | Prix total | |
|---|---|---|---|
| 60 | €0,81 | €48,48 | |
| 90 | €0,72 | €64,65 | |
| 120 | €0,67 | €80,81 | |
| 180 | €0,63 | €113,98 | |
| 270 | €0,61 | €164,17 | |
| 360 | €0,59 | €211,80 |
Diflucan 100 mg
| Quantité | Prix par comprimé | Prix total | |
|---|---|---|---|
| 30 | €1,45 | €43,38 | |
| 60 | €1,09 | €65,50 | |
| 90 | €0,97 | €87,61 | |
| 120 | €0,91 | €109,73 | |
| 180 | €0,85 | €153,11 | |
| 270 | €0,81 | €218,60 |
Diflucan 150 mg
| Quantité | Prix par comprimé | Prix total | |
|---|---|---|---|
| 30 | €1,84 | €55,29 | |
| 60 | €1,38 | €82,51 | |
| 90 | €1,22 | €109,73 | |
| 120 | €1,15 | €137,80 | |
| 180 | €1,07 | €192,24 | |
| 270 | €1,02 | €274,74 |
Diflucan 200 mg
| Quantité | Prix par comprimé | Prix total | |
|---|---|---|---|
| 30 | €2,89 | €86,76 | |
| 60 | €2,10 | €125,89 | |
| 90 | €1,82 | €164,17 | |
| 120 | €1,69 | €203,29 | |
| 180 | €1,55 | €279,85 | |
| 270 | €1,47 | €397,23 |
Diflucan 400 mg
| Quantité | Prix par comprimé | Prix total | |
|---|---|---|---|
| 30 | €4,82 | €144,60 | |
| 60 | €3,62 | €216,90 | |
| 90 | €3,22 | €290,05 | |
| 120 | €3,03 | €363,21 | |
| 180 | €2,83 | €508,66 | |
| 270 | €2,69 | €726,41 |
Paiement & livraison
Votre commande est soigneusement emballée et expédiée sous 24 heures. Voici à quoi ressemble généralement un colis.
De la taille d'une lettre personnelle classique (24x11x0,7 cm), sans aucune indication sur son contenu.



| Mode de livraison | Livraison estimée |
|---|---|
| Express Gratuit dès €300,00 | Livraison estimée vers la France : 4-7 jours |
| Standard Gratuit dès €200,00 | Livraison estimée vers la France : 14-21 jours |









Coupons de réduction
- Jour de l'An - 1 janvier 2026 9% NOUVELAN9
- Fête du Travail - 1 mai 2026 6% TRAVAIL6
- Fête de la Victoire - 8 mai 2026 6% VICTOIRE6
- Fête nationale (14 juillet) - 14 juillet 2026 9% BASTILLE9
- Assomption - 15 août 2026 6% ASSOMPTION6
- La Toussaint - 1 novembre 2026 6% TOUSSAINT6
- Jour de l'Armistice - 11 novembre 2026 7% ARMISTICE7
- Réveillon de Noël - 24 décembre 2026 9% REVEILLON9
- Noël - 25 décembre 2026 10% NOEL10
- Réveillon du Nouvel An - 31 décembre 2026 8% SAINTSYLVESTRE8
Noms de marque
| Pays | Noms de marque |
|---|---|
 Allemagne Allemagne | Canex Canifug Fluco Fluc Flucobeta Flucoderm FlucoLich Flunazul Fungata |
 Argentine Argentine | Candimicol Damicol Femixol Flucoginkan Fluconovag Fluzol Fungicil Fungocina Fungototal Honguil Plus Klonarizol Klonazol Micolis Novo Mutum Naxo C Nifurtox Niofen Periplum Ponaris Proseda F Triflucan |
 Australie Australie | Dizole Fluzole Ozole |
 Belgique Belgique | Candizole Fungimed |
 Brésil Brésil | Candix Candizol Celozol Farmazol Floltec Flucanil Flucanol Flucazol Flucocin Flucodan Flucoltrix Flucomed Fluconal Fluconax Fluconeo Fluconid Flucozen Flucozix Flunal Flunazol Fluotec Flusan Flutec Fungnon Glyflucan Helmicin Lertus Monipax Pantec Pronazol Riconazol Teczol Triazol Unizol Zelix Zolanix Zolmic Zolstatin Zoltec Zoltren |
 Danemark Danemark | Conasol Fungal |
 Espagne Espagne | Citiges Lavisa Loitin Nesporac Solacap |
 France France | Beagyne Triflucan |
 Grèce Grèce | Azoflu Azzol-S Dalrich Falipan Farviron Figalol Flucalit Flucocaps Flucodrug Flucofin Fluconapen Flucoran Flucozol Flukatril Flusenil Fluzomic Fumecal Funadel Fungo Fungram Fungustatin Fungusteril Fuxilidin Gynosant Hadlinol Medoflucon Mycazole Neomycol Opumyk Rifagen Stabilanol Tierlite Varmec Zidonil |
 Hongrie Hongrie | Dermyc Diflazon Flucohexal Flucoric Mycosyst Nofung |
 Italie Italie | Biozolene Elazor Flumicon Lefunzol Riflax Winch |
 Malaisie Malaisie | Avezol Biozole Flucon Fluconol Flucoric Flugal Fukole Medoflucon Odaft Stalene Zolstan |
 Mexique Mexique | Afungil Bioxel Candizol Difusel Fectrin Fharder Fleridux Flucoxan Fludisol Fluhexal Flukenol Flukezol Fluxes Fluxicap Fluzor Funser Lanfluzol Menifar Neofomiral Ongicil Oxifungol Ranflu Solarisol Terplex Waynazol Zilrin Zoldicam Zonal |
 Nouvelle-Zélande Nouvelle-Zélande | Canesten Fluconazole Flucazole |
 Pays-Bas Pays-Bas | Flucoderm |
 Pologne Pologne | Flucofast FlucoLEK Fluconazin Flumycon Mycomax Mycosyst |
 Portugal Portugal | Azoflune Fludocel Maxflin Reforce Supremase |
 République tchèque République tchèque | Diflazon Fluco Forcan Mycomax Mycosyst Mykohexal |
 Turquie Turquie | Biocanol Candidin Flucan Fluzole Fungan Kandizol Lumen Triflucan Trizol Zolax |
| Fabricant | Noms de marque |
|---|---|
| Cipla Limited | FCN Flucalup Forcan FZ |
| Inc. | FCN Flucalup Forcan FZ |
| Intas Pharmaceuticals Ltd. | FCN Flucalup Forcan FZ |
| Lupin Pharmaceuticals | FCN Flucalup Forcan FZ |
| Zenlabs Pharmaceutical Inc. | FCN Flucalup Forcan FZ |
Description
Le fluconazole est un antifongique largement utilisé pour traiter les mycoses à levures et d'autres infections fongiques. Il agit en empêchant la croissance du champignon dans l'organisme. Il existe à différents dosages et est souvent prescrit lorsqu'un traitement oral efficace et pratique est nécessaire.
Utilisations
Le fluconazole est utilisé pour traiter les candidoses oropharyngées, œsophagiennes ou vulvovaginales, ainsi que d'autres infections candidosiques systémiques graves (par ex., infections urinaires, péritonite, candidémie, candidose disséminée, méningite, pneumonie). Il est également utilisé pour traiter la méningite causée par Cryptococcus neoformans, ainsi que la blastomycose, la coccidioïdomycose et l'histoplasmose.

Le fluconazole a aussi été utilisé pour des infections moins sévères, comme les mycoses superficielles, les dermatophytoses et l'onychomycose. En outre, il est employé pour prévenir certaines infections fongiques graves (par ex., coccidioïdomycose, cryptococcose, candidose mucocutanée) chez les patients infectés par le virus de l'immunodéficience humaine (VIH), ainsi que chez d'autres personnes immunodéprimées (par ex., patients atteints de cancer, patients ayant reçu une greffe de moelle osseuse).
Avant de commencer un traitement par fluconazole, il faut prélever des échantillons adaptés pour culture fongique et réaliser les examens de laboratoire utiles (par ex., sérologie, histopathologie) afin d'isoler et d'identifier le ou les micro-organismes en cause. Le traitement par fluconazole peut être débuté en attendant les résultats de ces examens in vitro ; une fois les résultats disponibles, il doit toutefois être adapté en conséquence. Si des tests de sensibilité au fluconazole in vitro sont réalisés, leurs résultats doivent être interprétés avec prudence, car les tests actuellement disponibles peuvent ne pas refléter avec précision l'activité du fluconazole in vivo.
Infections candidales
Candidoses oropharyngées et œsophagiennes
Le fluconazole par voie orale ou IV est utilisé dans le traitement de la candidose oropharyngée chez les adultes immunodéprimés atteints du syndrome d'immunodéficience acquise (SIDA), d'un complexe relié au SIDA avancé (ARC), d'un cancer ou d'une autre maladie grave sous-jacente. Il est aussi utilisé par voie orale ou IV pour traiter la candidose œsophagienne chez les adultes atteints de SIDA, de cancer ou d'autres maladies graves sous-jacentes, y compris la sclérodermie systémique progressive.
Le fluconazole semble être au moins aussi efficace que les autres antifongiques utilisés en traitement initial des candidoses oropharyngées et/ou œsophagiennes, et dans certains cas plus efficace. Il est considéré comme un traitement de choix pour ces infections.
Le fluconazole a permis une disparition clinique des signes et symptômes de l'infection chez 79 à 100 % des patients atteints de candidose oropharyngée ; en revanche, une guérison microbiologique a généralement été obtenue chez 44 à 87 % des patients, et le taux de rechute peut être élevé, surtout chez les patients neutropéniques. Chez les adultes présentant une candidose œsophagienne confirmée par endoscopie, le fluconazole a entraîné une disparition clinique des signes et symptômes de l'infection chez environ 61 à 93 % des patients. Dans une étude menée chez des adultes atteints de candidose œsophagienne et de sclérodermie systémique progressive, le traitement par fluconazole a permis des guérisons mycologiques chez environ 93 % des patients en 2 à 4 semaines. Cependant, le taux de rechute atteignait presque 100 % dans les 3 mois suivant l'arrêt du traitement par fluconazole.
Les patients infectés par le VIH présentant des épisodes sévères ou récurrents de candidose oropharyngée ou œsophagienne peuvent bénéficier d'un traitement suppressif ou d'entretien à long terme (prophylaxie secondaire) afin de prévenir les rechutes.
Certains cliniciens considèrent le clotrimazole oral topique ou la nystatine orale comme le traitement de choix de la candidose oropharyngée non compliquée chez les patients infectés par le VIH. Ils recommandent de réserver les antifongiques systémiques (par ex., fluconazole oral, itraconazole oral, kétoconazole oral) aux candidoses oropharyngées qui ne répondent pas au traitement topique ainsi qu'aux formes sévères avec atteinte œsophagienne. Cependant, d'autres cliniciens préfèrent utiliser d'emblée un antifongique azolé oral.
Le fluconazole oral ou la solution buvable d'itraconazole est au moins aussi efficace qu'un traitement topique. Dans une étude menée chez des adultes infectés par le VIH atteints de candidose oropharyngée, les taux de réponse et d'éradication mycologique après 14 jours de traitement étaient respectivement de 100 et 75 % chez les patients recevant du fluconazole oral (100 mg une fois par jour), contre 65 et 20 % chez ceux recevant du clotrimazole topique (pastille orale de 10 mg 5 fois par jour). Dans une autre étude, 14 jours de traitement par fluconazole oral (100 mg une fois par jour en suspension buvable) se sont montrés plus efficaces que 14 jours de nystatine topique (500 000 unités en suspension buvable 4 fois par jour). Le taux de guérison mycologique était de 60 % dans le groupe fluconazole et de 6 % dans le groupe nystatine, et le taux de rechute à J42 était respectivement de 27 et 11 %. Après un suivi prolongé, l'efficacité comparative du fluconazole et d'autres antifongiques doit encore être mieux étudiée.
Un traitement anti-infectieux systémique est nécessaire en cas de candidose œsophagienne. Certains cliniciens estiment qu'un traitement de 14 à 21 jours par fluconazole oral (100 mg une fois par jour) ou par solution buvable d'itraconazole (200 mg une fois par jour) est très efficace dans cette indication, tandis que le kétoconazole oral l'est moins. Ils suggèrent d'utiliser une solution buvable d'itraconazole chez les patients qui ne répondent pas au fluconazole oral. L'amphotéricine B IV peut être utilisée chez les patients présentant une maladie réfractaire. Dans une étude randomisée, multicentrique, en double aveugle, comparant le fluconazole oral (dose initiale de 100 mg/jour augmentée à 200 mg/jour en l'absence d'amélioration symptomatique dans 1 à 2 semaines) pendant 8 semaines au kétoconazole oral (dose initiale de 200 mg/jour augmentée à 400 mg/jour en l'absence d'amélioration symptomatique dans 1 à 2 semaines) chez des patients atteints du SIDA avec candidose œsophagienne confirmée par endoscopie, la guérison endoscopique et la disparition des symptômes œsophagiens sont survenues respectivement chez 91 % et 85 % des patients sous fluconazole, contre 52 % et 65 % des patients sous kétoconazole ; les résultats d'une autre étude chez des patients immunodéprimés atteints de candidose œsophagienne indiquent que la durée du traitement initial peut être plus courte avec le fluconazole qu'avec le kétoconazole.
Candidose vulvovaginale
Le fluconazole oral est utilisé pour traiter la candidose vulvovaginale non compliquée, ainsi que la candidose vulvovaginale compliquée chez les femmes non enceintes. Avant de commencer un traitement antifongique chez une femme présentant des signes et symptômes de candidose vulvovaginale non compliquée, le diagnostic doit être confirmé soit par la mise en évidence de levures ou de pseudohyphes au microscope à partir d'un prélèvement vaginal (examen à l'état frais avec KOH à 10 % ou coloration de Gram), soit par culture. L'identification de Candida par culture en l'absence de symptômes ne justifie pas un traitement antifongique, car environ 10 à 20 % des femmes hébergent Candida ou d'autres levures dans le vagin. Chez les femmes souffrant de candidose vulvovaginale récurrente, des cultures vaginales doivent être réalisées pour confirmer le diagnostic et identifier des espèces inhabituelles de Candida (par ex., C. glabrata).
Candidose vulvovaginale non compliquée
Le fluconazole oral traite efficacement la candidose vulvovaginale non compliquée lorsqu'il est administré en dose unique. Une dose orale unique de 150 mg de fluconazole permet d'obtenir des guérisons cliniques (c'est-à-dire absence de brûlures vulvovaginales, de prurit, de gonflement, d'érythème, d'excoriations, de dyspareunie et/ou d'ulcérations, avec diminution importante des pertes vaginales) 5 à 16 jours après la prise chez environ 90 à 100 % des femmes non enceintes atteintes de candidose vulvovaginale non compliquée, et des guérisons mycologiques chez environ 77 à 100 % d'entre elles. Entre 27 et 62 jours après cette dose unique, les taux de guérison clinique et mycologique sont de 61 à 90 %, et le taux de rechute, de réinfection ou de recolonisation est d'environ 23 %. Plusieurs études chez des patientes atteintes de candidose vulvovaginale non compliquée suggèrent qu'une dose orale unique de 150 mg de fluconazole est aussi efficace que des schémas à doses multiples de clotrimazole, d'éconazole, de miconazole ou de terconazole par voie intravaginale. De plus, le schéma en dose unique orale de fluconazole est aussi efficace que l'itraconazole oral ou le kétoconazole oral dans la candidose vulvovaginale non compliquée.
Dans des études contrôlées chez des patientes atteintes de candidose vulvovaginale, les taux de guérison clinique et mycologique à 14 jours puis à 30-35 jours étaient similaires chez les patientes recevant du fluconazole oral (dose unique de 150 mg) et chez celles recevant du clotrimazole intravaginal (comprimé vaginal de 100 mg une fois par jour pendant 7 jours) ou du miconazole (crème vaginale de 100 mg une fois par jour pendant 7 jours). À 14 jours, le taux de guérison clinique était d'environ 95 à 96 % avec le fluconazole et de 95 à 97 % avec le clotrimazole ou le miconazole intravaginaux, tandis que le taux de guérison mycologique était de 77 à 80 % avec le fluconazole et de 72 à 82 % avec le clotrimazole ou le miconazole intravaginaux. À 30-35 jours, le taux de guérison clinique était de 69 à 75 % avec le fluconazole et de 72 à 80 % avec le clotrimazole ou le miconazole intravaginaux, et le taux de guérison mycologique était de 61 à 63 % avec le fluconazole et de 57 à 63 % avec le clotrimazole ou le miconazole intravaginaux.
En France, la candidose vulvovaginale non compliquée (définie comme une infection légère à modérée, sporadique ou occasionnelle, probablement causée par C. albicans, ou survenant chez des femmes immunocompétentes) est généralement traitée par un antifongique azolé intravaginal (par ex., butoconazole, clotrimazole, miconazole, terconazole, tioconazole) selon un schéma à dose unique approprié ou une cure courte, ou par une dose orale unique de fluconazole. Ces schémas sont généralement associés à des taux de guérison clinique et mycologique de 80-90 % chez des femmes non enceintes, par ailleurs en bonne santé, présentant des infections non compliquées. Certains cliniciens estiment qu'une dose orale unique de fluconazole peut présenter un avantage par rapport au traitement intravaginal classique, car elle favorise l'observance et peut réduire ou éliminer les infections rectales concomitantes susceptibles de servir de source de réinfection. Lorsqu'on évalue les bénéfices et les risques potentiels des traitements oraux par rapport aux traitements intravaginaux, il faut tenir compte du risque de toxicité (par ex., hépatotoxicité) et des interactions médicamenteuses associés au traitement oral. La fréquence des effets indésirables est plus élevée chez les patients recevant une dose orale unique de fluconazole que chez ceux recevant un traitement intravaginal, ce qui doit également être pris en considération.
Candidose vulvovaginale compliquée et récidivante
Le fluconazole oral traite la candidose vulvovaginale compliquée, y compris les formes récurrentes et sévères. La candidose vulvovaginale compliquée se définit par des infections récurrentes ou sévères, causées par des espèces de Candida autres que C. albicans, ou survenant chez les femmes enceintes ou chez les femmes présentant des pathologies sous-jacentes telles qu'un diabète mal contrôlé, une débilité ou une immunosuppression.
Les schémas optimaux pour traiter la candidose vulvovaginale récurrente (généralement définie par 4 épisodes ou plus de candidose vulvovaginale symptomatique par an) n'ont pas été établis. Bien que chaque épisode causé par C. albicans puisse répondre à une dose unique de fluconazole oral ou à une courte cure d'antifongique intravaginal, une durée initiale plus longue peut être nécessaire pour obtenir une rémission mycologique, et un traitement d'entretien prolongé peut être requis pour prévenir les rechutes. En France, un schéma intensif initial de 7 à 14 jours d'antifongique azolé intravaginal ou un schéma en 2 doses de fluconazole oral (150 mg répétés 3 jours après) est généralement suivi d'un traitement antifongique d'entretien pendant 6 mois. Parmi les options d'entretien couramment utilisées figurent le clotrimazole intravaginal (500 mg une fois par semaine), le kétoconazole oral (100 mg une fois par jour), le fluconazole oral (100-150 mg une fois par semaine) ou l'itraconazole oral (400 mg une fois par mois ou 100 mg une fois par jour). Ces traitements d'entretien peuvent réduire efficacement les infections récurrentes ; toutefois, 30 à 40 % des femmes présenteront une récidive après l'arrêt du traitement d'entretien.
Le taux de réponse aux traitements antifongiques de courte durée est plus faible chez les patientes souffrant de candidose vulvovaginale sévère (c'est-à-dire érythème vulvaire étendu, œdème, excoriations et fissures). Soit un schéma en 2 doses de fluconazole oral (150 mg répétés 3 jours après), soit un traitement intravaginal par azolé pendant 7 à 14 jours est recommandé pour ces infections. Ces traitements plus longs peuvent également être nécessaires pour la candidose vulvovaginale chez les femmes présentant des pathologies sous-jacentes invalidantes (par ex., diabète mal contrôlé ou traitement par corticostéroïdes). La candidose vulvovaginale peut survenir plus souvent et être plus sévère chez les femmes infectées par le virus de l'immunodéficience humaine (VIH) que chez les femmes non infectées par le VIH. Ces infections ont été reconnues comme une manifestation précoce du syndrome d'immunodéficience acquise (SIDA) chez les femmes. Bien que le traitement optimal de la candidose vulvovaginale récidivante chez les femmes infectées par le VIH n'ait pas été établi, rien n'indique à ce jour que ces femmes répondent moins bien aux schémas antifongiques intravaginaux ou oraux habituellement recommandés pour le traitement de la candidose vulvovaginale. Par conséquent, le Centers for Disease Control and Prevention (CDC) et d'autres cliniciens recommandent que le traitement de la candidose vulvovaginale chez les femmes infectées par le VIH soit identique à celui des femmes non infectées par le VIH.
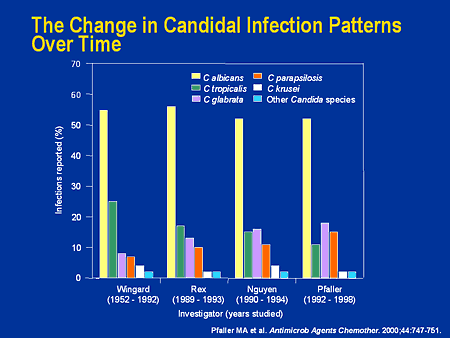
La candidose vulvovaginale récurrente peut rarement être causée par des souches résistantes de C. albicans ou, plus souvent, par d'autres espèces de Candida moins sensibles aux antifongiques azolés (par ex., C. glabrata). Il a été suggéré que le traitement répété de la candidose vulvovaginale récurrente par des antifongiques azolés intravaginaux, ainsi que l'utilisation généralisée et/ou inappropriée de ces agents en automédication, peuvent favoriser la sélection de Candida résistants aux azolés. Le traitement optimal des candidoses vulvovaginales causées par des Candida moins sensibles aux antifongiques azolés n'a pas été déterminé. En France, la candidose vulvovaginale causée par des espèces de Candida autres que C. albicans est généralement traitée pendant 7 à 14 jours par un antifongique autre que le fluconazole ; en cas de récidive, un traitement intravaginal par acide borique (capsule de 600 mg une fois par jour pendant 2 semaines) peut être envisagé. Une orientation vers un spécialiste est conseillée.
Candidémie et autres infections candidales
Le fluconazole s'est montré efficace dans le traitement d'infections candidales urinaires graves, de la péritonite et de la pneumonie. Il a également été efficace dans le traitement de la candidose mucocutanée chronique, de la candidémie, de la candidose disséminée chronique (candidose hépatosplénique), de l'endocardite candidosique, de la méningite candidosique, de l'ostéomyélite candidosique et d'autres infections candidales systémiques graves. Il a aussi été efficace dans le traitement de certaines infections candidales qui ne répondaient pas à l'amphotéricine B. Le fluconazole a été efficace pour traiter des infections candidales potentiellement mortelles chez des patients transplantés d'organes recevant un traitement immunosuppresseur. Chez certains receveurs de greffe rénale, le traitement par fluconazole a permis d'éliminer efficacement les infections fongiques sans interrompre ni réduire la dose du traitement immunosuppresseur.
L'amphotéricine B IV comme le fluconazole IV ou oral sont considérés comme des traitements de choix dans la candidose invasive systémique ; toutefois, il a été difficile de définir les schémas antifongiques optimaux pour ces infections, et chaque agent présente des limites. Bien que le fluconazole soit mieux toléré et plus facile à administrer que l'amphotéricine B IV, des souches de C. albicans résistantes au fluconazole sont isolées de plus en plus souvent chez des patients ayant déjà reçu du fluconazole, en particulier chez les patients infectés par le VIH. Certaines infections candidales (par ex., candidémie) sont de plus en plus causées par des souches intrinsèquement résistantes au fluconazole (par ex., C. krusei) ou susceptibles d'y être résistantes (par ex., C. glabrata). Le choix de l'antifongique pour le traitement initial des infections candidales invasives doit tenir compte des données épidémiologiques locales et/ou institutionnelles sur la prévalence des différentes souches de Candida et leurs profils de résistance, du statut de colonisation du patient, de la gravité et de la durée de la neutropénie ou de l'immunosuppression, ainsi que des antécédents de traitement par fluconazole. La plupart des cliniciens recommandent l'amphotéricine B IV si l'organisme infectant est connu ou suspecté être C. krusei ; en revanche, le fluconazole est préféré si l'infection est causée par C. lusitaniae.
Comme la candidémie est associée à une morbidité importante et à un risque de séquelles à long terme, un traitement antifongique est généralement recommandé chez tous les patients atteints de candidémie, qu'ils soient neutropéniques ou non, en plus du retrait et/ou du remplacement de tout cathéter intravasculaire. Il a été suggéré que le fluconazole oral pourrait être préféré à l'amphotéricine B IV pour traiter la candidémie chez les patients non neutropéniques, stables ou instables, sauf s'il existe des preuves que l'infection est due à des souches résistantes au fluconazole ou si le patient a déjà reçu ce traitement. L'amphotéricine B IV est généralement préférée pour traiter les candidémies sévères chez les patients infectés par des souches potentiellement résistantes au fluconazole (par ex., C. krusei, C. glabrata), chez les patients ayant récemment reçu du fluconazole et chez les patients immunodéprimés, notamment ceux infectés par le VIH. Dans une étude contrôlée chez des patients immunocompétents avec des taux normaux de neutrophiles, la réponse à un traitement conventionnel par amphotéricine B IV (pendant 7 jours, puis 3 fois par semaine pendant 10 jours supplémentaires) ou à un traitement par fluconazole (400 mg par jour administrés IV pendant 7 jours, puis par voie orale pendant 11 jours supplémentaires) était similaire. Les deux schémas semblaient également efficaces. Le taux global de réponse à un schéma conventionnel par amphotéricine B IV ou par fluconazole oral était aussi similaire dans une étude prospective randomisée incluant des patients neutropéniques et non neutropéniques atteints de candidose invasive documentée ou présumée. Cependant, des études complémentaires sont nécessaires pour mieux évaluer l'efficacité relative de l'amphotéricine B et du fluconazole chez les patients immunodéprimés ou atteints d'infections sévères.
Le fluconazole oral ou l'amphotéricine B IV sont recommandés lorsque le traitement de la candidurie est indiqué (par ex., patients symptomatiques ou neutropéniques, nourrissons de faible poids de naissance, patients transplantés rénaux, patients devant subir des gestes urologiques) ; le fluconazole peut être préféré sauf si l'infection est causée par C. krusei ou C. glabrata. L'irrigation vésicale par amphotéricine B conventionnelle a également été utilisée. Dans une étude randomisée menée chez des patients gériatriques hospitalisés présentant une fungurie causée par C. albicans, C. tropicalis ou C. glabrata, 5 jours d'irrigation vésicale par amphotéricine B conventionnelle (25 mg d'amphotéricine B dans 500 ml de solution de dextrose à 5 % perfusés via une sonde vésicale à un débit de 42 ml/heure) ou une cure de 5 jours de fluconazole oral (dose de charge de 200 mg le jour 1 suivie de 100 mg une fois par jour pendant 4 jours supplémentaires) ont permis d'éradiquer la fungurie chez 83 % et 66 % des patients, respectivement.
Le fluconazole est également utilisé en prophylaxie pour réduire l'incidence des candidoses chez les receveurs de greffe de moelle osseuse sous chimiothérapie ou radiothérapie. Il a aussi été utilisé en prophylaxie primaire contre les infections fongiques, y compris la candidose, chez un nombre limité de patients considérés comme à haut risque de développer de telles infections (par ex., patients neutropéniques atteints de cancer, colonisés par Candida et/ou recevant des corticostéroïdes, ainsi que certains patients atteints du SIDA).
Le fluconazole a donné de bons résultats chez plusieurs patients atteints d'endophtalmie à Candida. Cependant, des échecs de traitement ont aussi été rapportés, et sa place dans la prise en charge de cette infection reste à préciser. Des études chez le lapin montrent que le fluconazole diffuse dans l'œil et inhibe la croissance de C. albicans dans la choroïde, la rétine et le vitré lorsque le traitement IV est commencé dans les 24 heures suivant l'inoculation ; en revanche, il n'a pas inhibé efficacement la croissance du micro-organisme lorsque le traitement IV a été débuté 7 jours après l'inoculation, alors que l'infection était déjà bien installée.
Infections cryptococciques
Le fluconazole par voie orale ou IV est utilisé chez l'adulte immunocompétent ou immunodéprimé pour traiter la méningite due à C. neoformans. Il s'est montré efficace comme traitement initial de la méningite cryptococcique aiguë chez des adultes infectés ou non par le VIH. Il a permis une disparition clinique des signes et symptômes de l'infection chez environ 34 à 75 % de ces patients. Même si l'amphotéricine B, avec ou sans flucytosine, est généralement considérée comme le traitement initial de référence, le fluconazole peut être une alternative chez les patients dont la maladie n'est pas sévère, car il est en général bien toléré et atteint des concentrations élevées dans le liquide céphalorachidien. Bien que l'expérience chez l'enfant soit limitée, le fluconazole peut aussi être envisagé comme alternative à l'amphotéricine B dans cette tranche d'âge.
Le fluconazole s'est montré efficace dans le traitement de la méningite cryptococcique aiguë chez certains patients qui n'avaient pas répondu à l'amphotéricine B. Cependant, certaines données suggèrent qu'il pourrait être moins efficace que l'amphotéricine B au début du traitement chez les patients atteints du SIDA et entraîner une stérilisation plus lente du LCR. Dans une étude multicentrique randomisée comparant l'amphotéricine B (dose moyenne de 0,4-0,5 mg/kg/jour pendant 10 semaines, avec ou sans flucytosine) au fluconazole oral (400 mg le premier jour, puis 200-400 mg pendant 10 semaines) chez des patients atteints du SIDA présentant une méningite cryptococcique, le traitement a été efficace chez 40 % des patients recevant l'amphotéricine B et chez 34 % de ceux recevant le fluconazole. Bien que la mortalité globale ait été comparable entre les deux groupes (14 % versus 18 %), elle était plus élevée pendant les deux premières semaines chez les patients recevant le fluconazole (15 % contre 8 % avec l'amphotéricine B). Les cultures de LCR restaient positives en moyenne pendant environ 42 jours chez les patients traités par amphotéricine B, contre 64 jours chez ceux recevant le fluconazole. Dans une autre étude comparant l'amphotéricine B (0,7 mg/kg/jour pendant 1 semaine, suivie de cette dose 3 fois par semaine pendant 9 semaines, en association avec la flucytosine 150 mg/kg/jour) au fluconazole oral (400 mg/jour pendant 10 semaines) chez un nombre limité de patients VIH+ atteints de méningite cryptococcique, le traitement initial a été efficace chez tous les patients recevant l'amphotéricine B, mais chez seulement 43 % de ceux recevant le fluconazole ; les cultures de LCR restaient positives en moyenne pendant environ 16 et 41 jours selon le traitement reçu. Bien que les groupes aient été comparables sur la gravité de l'infection cryptococcique, le nombre de lymphocytes T CD4+ était plus faible dans le groupe fluconazole, ce qui rend l'interprétation plus difficile.
De nombreux cliniciens recommandent de commencer le traitement de la méningite cryptococcique chez les patients infectés par le VIH par un schéma d'amphotéricine B IV, avec flucytosine, pendant au moins 2 semaines, ou jusqu'à stabilisation de l'état du patient, puis de poursuivre par un traitement oral par fluconazole ou itraconazole pendant au moins 8-10 semaines, voire plus. En attendant davantage de données, certains estiment que le traitement initial par amphotéricine B IV, avec ou sans flucytosine, suivi d'un traitement d'entretien par fluconazole est l'approche la plus prudente, en particulier chez les patients présentant une maladie plus sévère ou à haut risque. À l'inverse, le traitement initial par fluconazole devrait probablement être réservé aux patients qui ne répondent pas à l'amphotéricine B, ne la tolèrent pas, ou ont une forme moins sévère de la maladie, par exemple sans manifestations neurologiques et avec de faibles titres d'antigène cryptococcique dans le LCR.
L'efficacité comparative d'un traitement d'attaque par amphotéricine B conventionnelle par voie intraveineuse, associée à la flucytosine (100 mg/kg/jour) ou à un placebo pendant 2 semaines, puis relayée par un traitement oral par fluconazole (800 mg/jour pendant 2 jours, puis 400 mg/jour pendant 8 semaines) ou par itraconazole (600 mg/jour pendant 3 jours, puis 400 mg/jour pendant 8 semaines), a été évaluée dans un essai multicentrique en double aveugle mené chez des patients atteints de méningite cryptococcique associée au SIDA.
À 2 semaines, les cultures du LCR étaient négatives chez 60 % des patients ayant reçu l'amphotéricine B avec la flucytosine, contre 51 % chez ceux ayant reçu l'amphotéricine B seule. La réponse clinique au fluconazole oral et à l'itraconazole oral pendant le traitement de relais était comparable. Cependant, le taux de stérilisation du LCR à 10 semaines était plus élevé chez les patients ayant reçu le fluconazole (72 %) que chez ceux ayant reçu l'itraconazole (60 %).
Une association de fluconazole oral (400 mg/jour pour les infections pulmonaires ou 400-800 mg/jour pour les infections du SNC) et de flucytosine orale (100-150 mg/kg/jour) a été utilisée comme alternative chez un nombre limité de patients atteints d'infections pulmonaires ou du SNC liées à une cryptococcose. Bien que cette association puisse être efficace dans les infections pulmonaires cryptococciques légères à modérées, elle s'est révélée inefficace chez certains patients atteints de méningite cryptococcique et n'est pas recommandée en traitement initial. De plus, chez des patients infectés par le VIH traités par fluconazole et flucytosine pour une méningite cryptococcique, ce schéma a été associé à une fréquence élevée d'effets indésirables, ayant conduit à l'arrêt de la flucytosine chez 28 % des patients.
Le taux de mortalité lors d'un premier épisode de méningite cryptococcique chez les patients atteints du SIDA est d'environ 25-58 % malgré un traitement par amphotéricine B. Chez les patients qui répondent au traitement antifongique initial, le taux de récidive de l'infection cryptococcique est de 35-65 %. Un traitement antifongique d'entretien, ou suppressif chronique, est généralement jugé nécessaire après le traitement initial, sauf en cas de restauration immunitaire liée à un traitement antirétroviral puissant.
Le fluconazole oral s'est montré efficace comme traitement d'entretien à long terme pour prévenir les rechutes de méningite cryptococcique chez les patients atteints du SIDA. Les résultats d'une étude multicentrique comparant la tolérance et l'efficacité du fluconazole oral (200 mg une fois par jour) à l'amphotéricine B IV (1 mg/kg une fois par semaine) pour prévenir les rechutes chez des patients atteints du SIDA dont les cultures cryptococciques étaient devenues négatives après un traitement initial adéquat par amphotéricine B indiquent que le schéma à base de fluconazole est plus efficace, pour prévenir les rechutes de méningite avec culture positive, et mieux toléré que le schéma à base d'amphotéricine B pour le traitement d'entretien. Dans une autre étude multicentrique comparant un traitement d'entretien par fluconazole oral (100-200 mg/jour) au placebo chez ces patients, le risque cumulatif global estimé de récidive cryptococcique, quel qu'en soit le site, après 1 an de traitement d'entretien par fluconazole était de 5 % versus 100 % avec le placebo.
L'efficacité du fluconazole d'entretien pour prévenir les rechutes cryptococciques chez les patients ayant une infection prostatique persistante après un traitement antifongique initial semble inférieure à celle observée globalement. Cette moindre efficacité peut toutefois être en partie compensée par une augmentation de la dose. Chez un nombre limité d'adultes VIH+ présentant une cryptococcose urinaire persistante, y compris des infections prostatiques, après un traitement initial adéquat par amphotéricine B, avec ou sans flucytosine, pour une méningite cryptococcique, un traitement d'entretien oral par fluconazole a permis une guérison mycologique chez la majorité des patients. À l'inverse, une rechute de la cryptococcose, avec massage prostatique, et/ou une infection systémique est survenue chez les autres patients pendant le traitement d'entretien par fluconazole.
La réponse, définie par une suppression prolongée du cryptococcus mise en évidence par le massage prostatique et l'absence de signe de rechute systémique ou du SNC, semble dépendre de la dose chez ces patients. Elle nécessite en général des doses orales de fluconazole de 200 à 600 mg par jour et peut mettre de plusieurs semaines à plusieurs mois à apparaître. Dans une étude, la probabilité de réponse était estimée à 36 % après 4 semaines et à 59 % après 27 semaines de traitement d'entretien. Des doses relativement élevées, par exemple 600 mg ou plus par jour, peuvent stériliser efficacement plusieurs gros abcès prostatiques chez certains patients. Cependant, les facteurs prédictifs de réponse et le traitement antifongique optimal dans cette situation restent à mieux définir. De plus, en raison du risque de rechute, certains cliniciens recommandent de rechercher soigneusement une localisation prostatique de l'infection chez tout patient de sexe masculin avant d'envisager un traitement d'entretien par fluconazole à faible dose.
Le fluconazole oral a été efficace chez un nombre limité de patients dans le traitement de cryptococcoses cutanées ou sous-cutanées. Il s'est aussi montré efficace dans le traitement de la pneumonie à cryptococcus chez un nombre limité de patients, même si une ablation chirurgicale du foyer infectieux a été nécessaire chez certains ; il faut toutefois garder à l'esprit qu'une pneumonie cryptococcique peut être la manifestation d'une infection disséminée.
Coccidioïdomycose
Le fluconazole oral a été utilisé avec succès dans le traitement de la coccidioïdomycose causée par Coccidioides immitis, par exemple en cas de méningite, d'infections pulmonaires ou d'infections disséminées touchant notamment les tissus mous, les os ou les articulations. Chez l'adulte atteint de méningite coccidioïdale, le fluconazole a entraîné une amélioration clinique et/ou paraclinique lorsqu'il a été utilisé seul ou en association avec l'amphotéricine B. Le fluconazole oral a été utilisé dans le traitement de la méningite coccidioïdale aussi bien chez des personnes infectées par le VIH que chez des personnes séronégatives. Comme il est généralement bien toléré et présente une pharmacocinétique favorable, notamment une forte diffusion dans le LCR après administration orale ou IV, il est considéré comme une alternative moins toxique à l'amphotéricine B dans le traitement de la méningite coccidioïdale et d'autres infections coccidioïdales persistantes, d'autant que ces infections nécessitent habituellement un traitement antifongique prolongé. Le fluconazole est considéré comme l'un des traitements de choix de la coccidioïdomycose ; néanmoins, l'amphotéricine B IV est généralement préférée en traitement initial des formes sévères, surtout chez les patients immunodéprimés, y compris ceux infectés par le VIH. D'autres études sont nécessaires pour évaluer son efficacité, préciser la dose orale optimale dans la coccidioïdomycose et déterminer s'il réduit réellement la morbidité et la mortalité. Certaines données suggèrent que le taux de réponse pourrait être meilleur avec des doses plus élevées de fluconazole, c'est-à-dire 400 mg/jour ou plus. Il a aussi été avancé que des doses relativement faibles, par exemple 50-100 mg/jour, pourraient favoriser le risque de rechute.
Blastomycose
Le fluconazole oral a été utilisé pour traiter la blastomycose causée par Blastomyces dermatitidis. Même si l'itraconazole oral ou l'amphotéricine B IV sont généralement considérés comme les traitements de choix, le fluconazole oral ou le kétoconazole oral peuvent être utilisés comme alternatives. L'amphotéricine B IV est généralement préférée pour les formes sévères, en particulier celles qui touchent le système nerveux central, ainsi que pour le traitement initial présumé de la blastomycose chez les patients immunodéprimés, y compris les personnes infectées par le VIH.
Des données suggèrent que l'itraconazole oral pourrait être plus efficace que le fluconazole oral ou le kétoconazole oral dans le traitement de la blastomycose. Plusieurs cliniciens considèrent l'itraconazole comme l'azolantifongique de choix dans les blastomycoses non méningées et non menaçant le pronostic vital, et le recommandent aussi comme traitement de relais chez les patients présentant des infections plus graves après une réponse initiale à l'amphotéricine B IV. Le fait que des échecs de traitement aient été rapportés avec un antifongique oral, par exemple le kétoconazole, dans la blastomycose cutanée ou pulmonaire chez des patients qui avaient une atteinte asymptomatique ou infraclinique du SNC au moment du diagnostic initial doit être pris en compte au moment de choisir un antifongique chez les patients atteints de blastomycose.
Histoplasmose
Le fluconazole oral a été utilisé avec un certain succès dans le traitement de l'histoplasmose causée par Histoplasma capsulatum. Même si l'amphotéricine B IV ou l'itraconazole oral sont considérés comme les traitements de choix, le fluconazole oral ou le kétoconazole oral sont considérés comme des alternatives. Le fluconazole oral (400-800 mg/jour) s'est montré efficace chez un nombre limité de patients VIH+ présentant une histoplasmose disséminée légère à modérément sévère ; toutefois, l'amphotéricine B IV est généralement préférée pour le traitement initial des formes sévères et mettant en jeu le pronostic vital, en particulier chez les patients immunodéprimés comme les personnes infectées par le VIH. Par ailleurs, l'itraconazole oral est habituellement l'azolantifongique privilégié pour traiter l'histoplasmose légère à modérée ou comme traitement de relais après une réponse à l'amphotéricine B dans les formes sévères.
Sporotrichose
Le fluconazole est utilisé comme traitement alternatif de la sporotrichose. L'amphotéricine B IV est habituellement considérée comme le traitement initial de choix dans les formes sévères ou mettant en jeu le pronostic vital, ainsi qu'en cas d'atteinte du système nerveux central ; l'itraconazole oral est considéré comme le traitement de choix dans les sporotrichoses cutanées, lymphocutanées, pulmonaires légères ou ostéoarticulaires, ainsi que comme traitement de relais après une réponse initiale à l'amphotéricine B IV. Le fluconazole est considéré comme un traitement de deuxième intention dans ces situations et, comme il pourrait être moins efficace que l'itraconazole, il ne devrait être utilisé que si le patient ne tolère pas l'itraconazole. Certains cliniciens estiment que le fluconazole n'est pas efficace et ne devrait pas être utilisé dans le traitement de la sporotrichose pulmonaire.
Aspergillose
Le fluconazole a été utilisé par voie orale, IV ou par perfusion intracavitaire chez quelques adultes pour traiter des pneumonies ou d'autres infections respiratoires dues à Aspergillus fumigatus, A. niger ou A. terreus. Dans une étude, le fluconazole a montré un taux d'efficacité clinique de 23-53 % dans les infections à Aspergillus et un taux de guérison mycologique d'environ 50 % pour les infections à A. fumigatus. Les résultats sont variables dans le traitement des infections à Aspergillus. L'amphotéricine B IV est généralement considérée comme le traitement de choix, et l'itraconazole comme l'alternative habituellement préférée pour traiter l'aspergillose.
Dermatophytoses
Le fluconazole oral s'est montré efficace dans le traitement de certaines dermatophytoses, par exemple la teigne du cuir chevelu, la teigne du corps, l'intertrigo inguinal et le pied d'athlète, causées par Epidermophyton, Microsporum ou Trichophyton. Il a aussi été efficace dans le traitement du pityriasis versicolor et de l'onychomycose.
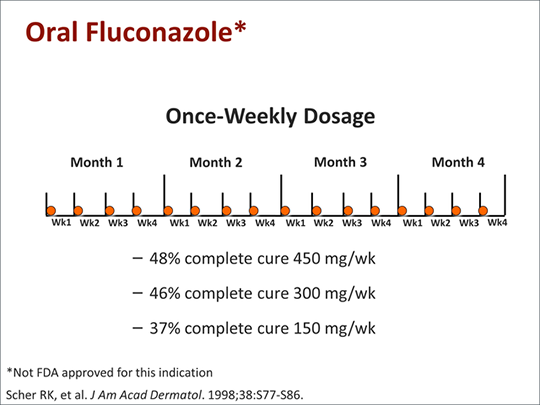
Le fluconazole oral (3-6 mg/kg/jour pendant 2-6 semaines) a efficacement traité la teigne du cuir chevelu chez des enfants âgés de 1,5 à 16 ans, avec une guérison clinique et mycologique chez environ 88-90 % des patients. Pour le traitement de la teigne du corps, de l'aine ou du pied chez l'adulte, le fluconazole oral a été efficace selon un schéma hebdomadaire de 150 mg une fois par semaine pendant 2-6 semaines. Des données indiquent que ce schéma hebdomadaire est aussi efficace que le schéma quotidien de 50 mg une fois par jour pour ces infections. Les résultats d'une étude randomisée montrent que le taux d'éradication à la fin du traitement chez des patients atteints de teigne du corps ou de l'aine était de 82-88 % avec le schéma hebdomadaire et de 94-100 % avec le schéma quotidien ; au suivi à 1 mois, les taux d'éradication globaux étaient respectivement de 91-100 % et 91-94 %. Bien que le schéma optimal du fluconazole oral dans l'onychomycose n'ait pas été établi, un traitement hebdomadaire, 150-450 mg une fois par semaine pendant 3-12 mois, s'est avéré efficace dans l'onychomycose de l'orteil chez un nombre limité d'adultes. Des études complémentaires sont nécessaires, et certaines données suggèrent que le fluconazole pourrait être moins efficace que l'itraconazole oral ou la terbinafine orale dans le traitement de l'onychomycose.
La teigne du corps et la teigne inguinale peuvent généralement être traitées efficacement par un antifongique local ; un traitement oral peut toutefois être nécessaire si la maladie est étendue, s'il existe une folliculite dermatophytique, si l'infection est chronique ou résistante au traitement local, ou si le patient est immunodéprimé ou présente une maladie associée. La teigne du cuir chevelu et la teigne de la barbe sont généralement traitées par voie orale. Même si les antifongiques locaux suffisent le plus souvent dans les formes simples de teigne des mains et des pieds, un traitement oral est indiqué en cas d'atteinte hyperkératosique des paumes et des plantes, dans les formes chroniques de pied d'athlète de type mocassin, sèches, et dans les onychomycoses.
Prévention des infections fongiques chez les personnes infectées par le VIH
Le fluconazole a été utilisé chez les personnes infectées par le VIH en prophylaxie primaire contre certaines infections fongiques sévères, par exemple la cryptococcose, ainsi que comme traitement suppressif ou d'entretien à long terme, c'est-à-dire en prophylaxie secondaire, pour prévenir la récidive de certaines infections fongiques comme la coccidioïdomycose, la cryptococcose ou la candidose mucocutanée.
En France, la prévention des infections opportunistes, y compris des infections fongiques, chez les personnes infectées par le VIH est généralement guidée par des recommandations nationales d'experts ainsi que par des directives internationales. Ces recommandations couvrent la prévention de l'exposition aux agents pathogènes opportunistes, la prévention des premières manifestations de la maladie et la prévention des récidives. La prophylaxie primaire visant à prévenir un premier épisode de candidose mucocutanée chez l'adulte, l'adolescent, le nourrisson et l'enfant infectés par le VIH n'est pas recommandée. Même si une prophylaxie primaire systématique contre la coccidioïdomycose, la cryptococcose ou l'histoplasmose chez les personnes infectées par le VIH n'est pas recommandée, une prophylaxie primaire contre la cryptococcose ou l'histoplasmose peut être envisagée chez certains patients soigneusement sélectionnés. Les adultes, adolescents, nourrissons et enfants infectés par le VIH qui ont terminé un traitement initial pour une coccidioïdomycose, une cryptococcose ou une histoplasmose documentée devraient recevoir un traitement suppressif ou d'entretien à long terme, c'est-à-dire une prophylaxie secondaire, afin de prévenir la récidive. De plus, les personnes infectées par le VIH qui présentent des récidives fréquentes ou sévères de candidose mucocutanée, oropharyngée, œsophagienne ou vaginale, peuvent bénéficier d'un traitement suppressif ou d'entretien à long terme.
En raison des inquiétudes liées à l'utilisation d'antifongiques azolés oraux pendant la grossesse, le fluconazole ne doit pas être utilisé en prophylaxie primaire ni comme traitement suppressif ou d'entretien chronique chez la femme enceinte. Si une femme enceinte recevant une prophylaxie par fluconazole décide de poursuivre sa grossesse, cette prophylaxie doit être arrêtée. Une contraception efficace est recommandée chez toutes les femmes infectées par le VIH recevant un antifongique azolé oral comme traitement suppressif. L'amphotéricine B IV conventionnelle peut être préférée lorsqu'un traitement d'entretien à long terme contre la coccidioïdomycose, la cryptococcose ou l'histoplasmose est nécessaire chez une femme enceinte infectée par le VIH, en particulier pendant le premier trimestre.
Prophylaxie primaire
Coccidioïdomycose
La prophylaxie primaire systématique contre la coccidioïdomycose n'est généralement pas recommandée chez les patients infectés par le VIH vivant dans des zones d'endémie. Certains cliniciens estiment qu'elle pourrait être envisagée chez les personnes infectées par le VIH ayant une sérologie CF positive, mais sans maladie active. Il reste toutefois incertain qu'une prophylaxie primaire apporte un bénéfice chez les patients vivant dans les zones d'endémie. Des cas de coccidioïdomycose active ont été rapportés chez des personnes VIH+ recevant un traitement azolé pour d'autres affections. Le test cutané systématique chez les personnes VIH+ vivant dans les zones d'endémie n'est pas prédictif de la maladie et n'est généralement pas recommandé. Dans ces zones, une sérologie positive peut indiquer un risque accru d'infection active, mais le dépistage sérologique systématique ne semble pas utile et n'est généralement pas recommandé.
Cryptococcose
Bien qu'une prophylaxie primaire systématique contre la cryptococcose ne soit généralement pas recommandée, elle peut être envisagée chez les adultes et les adolescents infectés par le VIH ayant un taux de lymphocytes T CD4+ inférieur à 50/mm3, ainsi que chez les nourrissons et les enfants sévèrement immunodéprimés selon des critères adaptés à l'âge. Elle n'est pas recommandée en routine en raison de la relative rareté de la cryptococcose, de l'absence de bénéfice net démontré sur la survie, et des préoccupations concernant les interactions médicamenteuses, le risque de résistance et le coût. La nécessité d'une prophylaxie primaire ou d'un traitement suppressif contre d'autres infections fongiques, comme la coccidioïdomycose, l'histoplasmose ou la candidose mucocutanée, doit également être prise en compte dans la décision de mettre en place une prophylaxie contre la cryptococcose. Le dépistage systématique de l'antigène cryptococcique sérique chez les personnes asymptomatiques n'est pas recommandé, car il est peu probable qu'il modifie la prise en charge clinique. Les personnes infectées par le VIH ne peuvent pas éviter complètement l'exposition à Cryptococcus neoformans, et rien ne prouve que l'exposition aux fientes de pigeon augmente le risque de cryptococcose.
Le fluconazole par voie orale est le traitement de référence pour la prophylaxie primaire de la cryptococcose chez les adultes, les adolescents, les nourrissons et les enfants vivant avec le VIH. L'itraconazole par voie orale (en gélules) est considéré comme une alternative.
Histoplasmose
Une prophylaxie primaire de l'histoplasmose peut être envisagée chez les adultes ou les adolescents vivant avec le VIH ayant un taux de lymphocytes T CD4+ inférieur à 100/mm3 et exposés à un risque particulièrement élevé de contact avec Histoplasma capsulatum, en raison d'une exposition professionnelle ou du lieu de résidence dans une zone hyperendémique (au moins 10 cas/100 patients-année). Elle peut aussi être envisagée chez les nourrissons ou les enfants vivant avec le VIH présentant une immunodépression sévère et vivant dans une zone d'endémie. Pour décider de mettre en place une prophylaxie primaire chez ces patients, les cliniciens doivent prendre en compte l'incidence locale de l'histoplasmose, le risque d'interactions médicamenteuses, la toxicité, le développement de résistances, le coût, ainsi que la nécessité éventuelle d'une prophylaxie contre d'autres infections fongiques comme la candidose ou la cryptococcose.
Le traitement privilégié pour la prophylaxie primaire de l'histoplasmose chez les adultes, les adolescents ou les enfants vivant avec le VIH est l'itraconazole par voie orale (gélules) ; aucune alternative spécifique à l'itraconazole n'est généralement recommandée. Certaines données laissent penser que le fluconazole par voie orale pourrait être inefficace pour prévenir un premier épisode d'histoplasmose.
Candidose mucocutanée
La prophylaxie primaire visant à prévenir un premier épisode de candidose mucocutanée (œsophagienne, oropharyngée, vaginale) chez les adultes, les adolescents, les nourrissons ou les enfants vivant avec le VIH n'est généralement pas recommandée. Cela s'explique par la bonne prise en charge de ces infections aiguës, leur caractère rarement mortel, ainsi que par les inquiétudes liées au développement possible de résistances, aux interactions médicamenteuses potentielles et au coût d'une prophylaxie antifongique.
Prévention des récidives
Coccidioïdomycose
Les personnes vivant avec le VIH qui ont terminé le traitement initial d'une coccidioïdomycose documentée doivent recevoir un traitement suppressif ou d'entretien au long cours (prophylaxie secondaire) afin de prévenir une récidive ou une rechute. Le fluconazole par voie orale est généralement considéré comme le traitement de choix, avec l'amphotéricine B IV et l'itraconazole par voie orale (en gélules) comme alternatives. Le traitement suppressif au long cours pour prévenir une récidive ou une rechute de coccidioïdomycose chez les adultes, les adolescents, les nourrissons et les enfants vivant avec le VIH est généralement poursuivi à vie. Même si le risque de récidive des infections fongiques systémiques peut être faible chez les patients dont le taux de lymphocytes T CD4+ dépasse 100/mm3 sous traitement antirétroviral combiné efficace, les données disponibles restent insuffisantes pour formuler une recommandation claire sur l'arrêt de la prophylaxie contre la coccidioïdomycose chez ces patients.
Cryptococcose
Les personnes vivant avec le VIH qui ont terminé le traitement initial d'une cryptococcose documentée doivent recevoir un traitement suppressif ou d'entretien au long cours (prophylaxie secondaire) pour prévenir une récidive ou une rechute, sauf en cas de récupération immunitaire sous traitement antirétroviral combiné efficace. Le fluconazole par voie orale est généralement considéré comme le traitement de choix, avec l'amphotéricine B IV et l'itraconazole par voie orale (en gélules) comme alternatives. Les résultats d'une étude randomisée, en double aveugle et contrôlée menée chez des personnes vivant avec le VIH atteintes d'une méningite cryptococcique documentée et correctement traitée suggèrent que le fluconazole par voie orale (200 mg une fois par jour) est plus efficace que l'itraconazole par voie orale (200 mg une fois par jour) en traitement suppressif, avec des taux de rechute à culture positive de 4 % sous fluconazole contre 23 % sous itraconazole.

Le traitement suppressif ou d'entretien pour prévenir une récidive ou une rechute de cryptococcose chez les personnes vivant avec le VIH est généralement poursuivi à vie, sauf en cas de récupération immunitaire sous traitement antirétroviral combiné efficace. Des données limitées indiquent que l'arrêt de ce traitement chez les adultes et les adolescents vivant avec le VIH, après la fin du traitement initial de la cryptococcose, sans symptômes, et avec un taux de lymphocytes T CD4+ maintenu au-dessus de 100-200/mm3 pendant au moins 6 mois en réponse au traitement antirétroviral, est associé à un faible risque de récidive. Sur cette base, et au vu de l'expérience plus large concernant l'arrêt en toute sécurité des traitements suppressifs au long cours pour d'autres infections opportunistes, il peut être raisonnable d'envisager l'arrêt du traitement suppressif chez les patients remplissant ces critères. Des récidives peuvent toutefois survenir après l'arrêt du traitement, et le traitement suppressif doit être repris si le taux de lymphocytes T CD4+ redescend en dessous de 100-200/mm3. La sécurité de l'arrêt de ce traitement chez les nourrissons et les enfants vivant avec le VIH n'a pas été étudiée, et les enfants doivent recevoir un traitement suppressif à vie après un épisode de cryptococcose.
Histoplasmose
Pour le traitement suppressif au long cours chez les patients vivant avec le VIH présentant une histoplasmose documentée et correctement traitée, l'itraconazole par voie orale (en gélules) est généralement considéré comme le traitement de choix, et l'amphotéricine B IV comme alternative.
Candidose mucocutanée
Un traitement suppressif ou d'entretien au long cours doit être envisagé chez les adultes et les adolescents ayant des antécédents de candidose œsophagienne documentée, en particulier en cas d'épisodes multiples, en tenant compte du risque de développement de souches de Candida résistantes. Ce traitement doit aussi être envisagé chez les nourrissons et les enfants présentant une candidose mucocutanée sévère et récidivante, notamment une candidose œsophagienne. Bien que de nombreux experts déconseillent la prophylaxie primaire au long cours contre les candidoses oropharyngées ou vulvovaginales récidivantes chez les patients vivant avec le VIH, pour les mêmes raisons que la prophylaxie primaire systématique, un traitement suppressif peut être envisagé chez les personnes ayant des récidives fréquentes ou sévères de ces infections. Les éléments à prendre en compte comprennent l'impact des récidives sur le bien-être et la qualité de vie du patient, la nécessité d'une prophylaxie contre d'autres infections fongiques, le coût de la prophylaxie, la toxicité des médicaments, les interactions médicamenteuses et le risque de développement de résistances chez Candida et d'autres champignons.
Si un traitement suppressif au long cours est indiqué pour prévenir la candidose mucocutanée chez les adultes, les adolescents, les nourrissons ou les enfants vivant avec le VIH présentant des récidives fréquentes ou sévères de candidose oropharyngée, œsophagienne ou vaginale, le fluconazole par voie orale est généralement considéré comme le traitement de choix, et l'itraconazole (en solution buvable) comme alternative.
Le traitement suppressif au long cours pour prévenir la récidive ou la rechute des infections fongiques chez les patients vivant avec le VIH est généralement poursuivi à vie. Chez certains patients vivant avec le VIH ayant reçu du fluconazole par voie orale pour prévenir la récidive d'une candidose oropharyngée pendant une médiane de 18 mois (extrêmes : 4-98 mois) sous traitement antirétroviral combiné efficace, l'arrêt du traitement suppressif par fluconazole oral a entraîné une récidive de candidose oropharyngée chez seulement 10 % des patients dans les 6 à 11 mois. Même si les patients vivant avec le VIH recevant une prophylaxie antifongique suppressive peuvent présenter un faible risque de récidive d'infections fongiques lorsque leur taux de lymphocytes T CD4+ dépasse 100/mm3 sous traitement antirétroviral combiné efficace, les données actuelles restent insuffisantes pour recommander clairement l'arrêt de la prophylaxie chez ces patients.
Prévention des infections fongiques chez les patients transplantés et atteints de cancer
Le fluconazole est utilisé en prophylaxie pour réduire l'incidence des candidoses chez les patients recevant une greffe de moelle osseuse (GMO) et traités par chimiothérapie ou radiothérapie. Il a aussi été utilisé pour prévenir les infections fongiques chez les patients ayant subi une transplantation hépatique et chez les patients atteints de cancer considérés à risque de neutropénie et d'infections fongiques. Certaines données indiquent que la prophylaxie par fluconazole chez les patients transplantés et les patients atteints de cancer peut réduire la fréquence des candidoses oropharyngées et/ou systémiques pendant la période précédant la récupération des neutrophiles. En outre, la prophylaxie par fluconazole peut diminuer le recours à un traitement antifongique empirique chez ces patients. L'efficacité du fluconazole par voie orale (400 mg une fois par jour) en prophylaxie des infections fongiques chez les patients neutropéniques a été évaluée dans une étude randomisée contre placebo incluant 274 patients atteints de cancer, âgés de 18 à 80 ans, recevant une chimiothérapie cytotoxique ou un traitement de conditionnement pour GMO. La proportion de patients n'ayant pas eu besoin d'un traitement empirique par amphotéricine B IV était similaire dans les deux groupes (57 % sous fluconazole et 50 % sous placebo). En revanche, un succès complet sans colonisation fongique a été observé chez 37 % des patients sous fluconazole contre 20 % sous placebo. De plus, l'incidence des infections fongiques superficielles était plus faible chez les patients recevant du fluconazole (7 %) que chez ceux recevant le placebo (18 %), et seulement 3 % des patients sous fluconazole ont développé des infections fongiques invasives confirmées, contre 17 % sous placebo. Bien que la prophylaxie par fluconazole n'ait pas modifié la mortalité globale, l'analyse en intention de traiter montre que le nombre de décès attribués à une infection fongique invasive confirmée était plus faible dans le groupe fluconazole (1 sur 15) que dans le groupe placebo (6 sur 15).
L'utilisation d'une prophylaxie antifongique primaire chez les patients atteints de cancer recevant un traitement myélosuppresseur, ou chez les patients bénéficiant d'une GMO ou d'une transplantation d'organe solide, reste controversée, notamment parce qu'elle peut favoriser la colonisation par des champignons résistants et/ou l'émergence d'organismes hautement résistants. Des études rétrospectives ont montré un risque accru de colonisation par Candida krusei chez les receveurs de GMO et chez les patients neutropéniques ayant reçu une prophylaxie par fluconazole ; dans l'une de ces études, environ 41 % des patients recevant du fluconazole présentaient une colonisation par C. krusei contre 17 % de ceux n'en recevant pas. Par conséquent, la plupart des cliniciens déconseillent généralement la prophylaxie antifongique primaire, sauf chez certains patients soigneusement sélectionnés à très haut risque, lorsque les bénéfices potentiels semblent l'emporter sur les risques possibles. De nombreux experts estiment toutefois que des études contrôlées et randomisées doivent continuer à évaluer l'utilisation du fluconazole pour prévenir les infections fongiques chez les patients atteints de cancer et les receveurs de GMO.
Posologie et administration
Le fluconazole est un antifongique triazolé utilisé dans les candidoses superficielles des muqueuses (oropharyngées, œsophagiennes ou vaginales) et les infections fongiques cutanées. Il est aussi utilisé dans les infections systémiques, notamment les candidoses systémiques, la coccidioïdomycose et la cryptococcose. Il a également été essayé dans la blastomycose, l'histoplasmose et la sporotrichose.
Le fluconazole est administré par voie orale ou intraveineuse à des doses comparables. En perfusion intraveineuse, il est administré sous forme de solution à 2 mg/mL à un débit de 5 à 10 mL/minute (300 à 600 mL/heure). En France, le débit maximal de perfusion doit être conforme aux informations du produit autorisé utilisé localement.
Pour la candidose muqueuse superficielle (hors candidose génitale), la dose orale habituelle de fluconazole en France est de 50 mg par jour. Toutefois, 100 mg par jour peuvent être administrés si nécessaire.
Le traitement dure généralement 7 à 14 jours pour la candidose oropharyngée (sauf chez les patients sévèrement immunodéprimés), 14 jours pour la candidose buccale atrophique associée au port de prothèses dentaires, et 14 à 30 jours pour les autres candidoses des muqueuses, y compris l'œsophagite. Des doses plus élevées sont recommandées aux États-Unis, où une dose initiale de 200 mg de fluconazole est suivie de 100 mg par jour. La durée minimale du traitement est de 14 jours pour l'infection oropharyngée, ou d'au moins 21 jours et au moins 14 jours après la disparition des symptômes pour les infections œsophagiennes ; des doses allant jusqu'à 400 mg par jour peuvent être utilisées si nécessaire en cas de candidose œsophagienne.
Administration orale
Le fluconazole peut être pris par voie orale pendant ou en dehors des repas. La poudre de fluconazole pour suspension buvable doit être reconstituée au moment de la délivrance en ajoutant 24 mL d'eau distillée ou purifiée dans le flacon contenant 0,35 ou 1,4 g de médicament, afin d'obtenir une suspension à 50 ou 200 mg/5 mL, respectivement. Le flacon doit être vigoureusement agité pour remettre la poudre en suspension ; la suspension doit aussi être bien agitée juste avant l'administration.
Administration IV
Les perfusions IV de fluconazole doivent être administrées une fois par jour à un débit ne dépassant pas 200 mg/heure. Les solutions de fluconazole destinées à la perfusion IV doivent être inspectées visuellement avant administration afin de vérifier l'absence de changement de couleur et de particules, lorsque la solution et le contenant le permettent. La solution pour perfusion IV doit être jetée si elle est trouble ou contient un précipité, ou si le sceau n'est pas intact. Les contenants Viaflex® Plus de fluconazole doivent être vérifiés pour détecter d'éventuelles microfuites en pressant fermement la poche. La solution doit être jetée si le sceau du contenant n'est pas intact, si des fuites sont détectées, ou si la solution est trouble ou contient un précipité. Aucun additif ne doit être introduit dans le contenant plastique de perfusion. La solution en contenant plastique ne doit pas être utilisée en connexion en série avec d'autres contenants plastiques, car cela pourrait provoquer une embolie gazeuse due à l'air résiduel aspiré du contenant principal avant la fin de l'administration du contenant secondaire.
Une dose orale unique de fluconazole 150 mg peut être utilisée en cas de candidose génitale (candidose vaginale ou balanite candidosique). Les dermatophytoses, le pityriasis versicolor et les infections cutanées à Candida peuvent être traités par fluconazole 50 mg par voie orale une fois par jour pendant une durée pouvant aller jusqu'à six semaines.
Les candidoses systémiques, les méningites cryptococciques et les autres infections cryptococciques peuvent être traitées par voie orale ou par perfusion intraveineuse avec le fluconazole. La dose initiale est de 400 mg, suivie de 200 à 400 mg par jour. La durée du traitement dépend de la réponse clinique et mycologique, mais elle est généralement d'au moins 6 à 8 semaines. Pour la méningite cryptococcique en France, la durée du traitement est déterminée par la réponse clinique et la stérilisation du LCR, et un traitement prolongé est généralement nécessaire.
Le fluconazole peut aussi être utilisé à des doses quotidiennes de 100 à 200 mg par voie orale ou intraveineuse pour prévenir une rechute après un traitement antifongique initial chez les patients atteints du SIDA présentant une méningite cryptococcique aiguë. Chez les patients immunodéprimés à risque d'infections fongiques, le fluconazole peut être administré en prophylaxie par voie orale ou en perfusion à raison de 50 à 400 mg par jour. Toutefois, une prophylaxie au long cours a été associée à l'émergence d'organismes résistants. Les doses chez les enfants de plus de 4 semaines sont de 3 mg/kg/jour pour les infections superficielles (une dose de charge de 6 mg/kg peut être utilisée le premier jour si nécessaire) et de 6 à 12 mg/kg/jour pour les infections systémiques. Une dose de 3 à 12 mg/kg/jour peut être administrée en prophylaxie chez les enfants immunodéprimés. Chez les nourrissons de moins de 2 semaines, toutes ces doses doivent être administrées une fois toutes les 72 heures. Chez ceux âgés de 2 à 4 semaines, elles doivent être administrées toutes les 48 heures.
La dose maximale de 400 mg par jour ne doit pas être dépassée chez les enfants, ni 12 mg/kg à intervalles appropriés chez les nourrissons. Une réduction de la posologie peut être nécessaire chez les patients présentant une insuffisance rénale.
Posologies élevées
Des patients atteints d'infections potentiellement mortelles causées par Candida spp., Cryptococcus neoformans et Coccidioides immitis ont été traités avec des doses supérieures à celles recommandées dans les informations du produit autorisé pour le fluconazole.
Des études de dose ont montré que des doses quotidiennes de 800 à 1000 mg de fluconazole sont efficaces et bien tolérées. Dans une étude menée chez 11 patients vivant avec le VIH, ayant reçu du fluconazole 800 à 1000 mg par jour en perfusion intraveineuse pendant 3 semaines, puis par voie orale jusqu'à négativation des cultures de LCR, 6 patients avaient répondu au traitement à 10 semaines, et 2 autres avaient montré une amélioration clinique. Des doses quotidiennes allant jusqu'à 800 mg ont été utilisées dans la blastomycose et la coccidioïdomycose, et des doses de 10 mg/kg/jour ont été essayées dans la candidose disséminée.
Posologies intermittentes
Des inquiétudes ont été exprimées au sujet de l'usage de plus en plus large du fluconazole, en particulier concernant l'impact d'un traitement continu chez les patients immunodéprimés sur le développement de résistances. Malgré cela, le fluconazole reste largement utilisé en prophylaxie primaire et secondaire. Certains investigateurs ont proposé des schémas intermittents, même si cela pourrait encore augmenter le risque d'infections dues à des organismes résistants. Un traitement hebdomadaire par fluconazole a été essayé dans l'onychomycose et la teigne du cuir chevelu.
Administration en cas d'insuffisance rénale
Les patients présentant une insuffisance rénale peuvent nécessiter une réduction de dose. Les doses de charge ou les doses initiales habituelles de fluconazole doivent être administrées le premier jour du traitement, puis les doses suivantes doivent être adaptées en fonction de la clairance de la créatinine (CC) :
- CC supérieure à 50 mL/minute : 100 % de la dose standard recommandée ;
- CC inférieure à 50 mL/minute et absence de dialyse : 50 % de la dose standard recommandée ;
- patients sous hémodialyse régulière : 100 % de la dose standard recommandée après chaque séance de dialyse. Aucun ajustement de dose n'est nécessaire chez les patients insuffisants rénaux recevant un traitement en dose unique.
Posologie chez l'adulte
Candidose oropharyngée et œsophagienne
Pour le traitement de la candidose oropharyngée ou œsophagienne, la posologie habituelle du fluconazole chez l'adulte est de 200 mg en dose unique le premier jour, suivis de 100 ou 200 mg une fois par jour. Des doses allant jusqu'à 400 mg une fois par jour peuvent être utilisées selon la réponse du patient. Même si les signes cliniques de la candidose oropharyngée disparaissent généralement en quelques jours après le début du traitement par fluconazole, le fabricant et certains cliniciens recommandent de poursuivre le traitement pendant au moins 2 semaines afin de réduire le risque de rechute.

Cependant, d'autres cliniciens contestent l'intérêt d'un traitement prolongé chez les patients atteints de cette infection. Les patients présentant une candidose œsophagienne doivent recevoir du fluconazole pendant au moins 3 semaines, et pendant au moins 2 semaines après la disparition des symptômes. La posologie optimale du traitement d'entretien chez les patients atteints de candidose oropharyngée n'a pas été établie. Des doses orales de 50 à 100 mg une fois par jour sont généralement utilisées avec succès pour le traitement d'entretien chez ces patients ; des doses allant jusqu'à 200 mg une fois par jour ont parfois été utilisées.
Candidose vulvovaginale
Pour traiter une candidose vulvovaginale non compliquée chez une femme non enceinte, la dose habituelle de fluconazole par voie orale est de 150 mg en prise unique. En cas de candidose vulvovaginale récidivante chez une femme non enceinte, 2 doses de 150 mg de fluconazole par voie orale doivent être administrées à 3 jours d'intervalle afin d'obtenir une rémission mycologique. Ensuite, un traitement d'entretien de 100 à 150 mg une fois par semaine doit être poursuivi pendant 6 mois pour prévenir les récidives. Un schéma en 2 doses de fluconazole par voie orale (2 doses de 150 mg administrées à 3 jours d'intervalle) est également recommandé pour traiter une candidose vulvovaginale sévère chez une femme non enceinte.
Leishmaniose
Le fluconazole a été essayé dans le traitement de la leishmaniose cutanée causée par Leishmania major. Dans une étude randomisée, en double aveugle, contrôlée par placebo, 80 patients ont reçu un traitement oral de 6 semaines par 200 mg de fluconazole par jour ; parmi eux, 63 ont obtenu une guérison complète des lésions après 3 mois, contre 22 sur 65 dans le groupe placebo. Cependant, d'autres études ont rapporté un taux de réponse qui ne différait pas significativement de celui du placebo.
Autres infections candidales
Pour traiter les candidoses systémiques, la dose habituelle chez l'adulte est de 400 mg en dose unique le premier jour, suivie de 200 mg une fois par jour. Chez un nombre limité de patients présentant des infections urinaires à Candida ou une péritonite candidosique, des doses de 50 à 200 mg par jour ont été utilisées. La posologie et la durée optimales du traitement chez les patients atteints de candidémie, de candidose disséminée ou de pneumonie n'ont pas été établies ; toutefois, un nombre limité de patients ont reçu des doses de fluconazole allant jusqu'à 400 mg par jour. Certains cliniciens recommandent une dose quotidienne de 400 à 800 mg de fluconazole chez les patients atteints de candidose invasive. Le traitement doit être poursuivi pendant au moins 4 semaines et au moins 2 semaines après la disparition des symptômes.
Infections cryptococciques
Pour traiter la méningite cryptococcique, la dose habituelle de fluconazole chez l'adulte est de 400 mg en dose unique le premier jour de traitement, suivie de 200 à 400 mg une fois par jour. Certaines données suggèrent qu'une dose de 400 mg est plus efficace que des doses plus faibles pour traiter cette infection. Une dose plus élevée de fluconazole (800 à 1000 mg par jour) a été utilisée chez certains patients vivant avec le VIH pour traiter la méningite cryptococcique. En traitement initial de la méningite cryptococcique, le fluconazole est habituellement poursuivi pendant 10 à 12 semaines après la stérilisation du LCR.

Coccidioïdomycose
Pour traiter la méningite coccidioïdale chez l'adulte, des doses de fluconazole de 200 à 800 mg une fois par jour ont été recommandées. Pour traiter la méningite coccidioïdale chez les patients atteints du SIDA, des doses de fluconazole de 400 à 800 mg par jour sont recommandées. Un traitement associé par amphotéricine B, administrée par voie intracisternale, intraventriculaire ou intrathécale, a été utilisé chez certains patients.
Blastomycose ou histoplasmose
Si le fluconazole est utilisé pour traiter la blastomycose ou l'histoplasmose, une dose quotidienne de 400 à 800 mg est recommandée.
Prévention des infections fongiques chez les personnes infectées par le VIH
En France, pour la prophylaxie primaire contre la cryptococcose chez les adultes ou adolescents infectés par le VIH avec des taux absolus de lymphocytes T auxiliaires/inducteurs (CD4+, T4+) inférieurs à 50/mm3, les recommandations spécialisées peuvent préconiser 100 à 200 mg de fluconazole par voie orale une fois par jour chez certains patients à haut risque.
Bien qu'il existe des données suggérant que le fluconazole oral à 400 mg une fois par semaine puisse être efficace en prophylaxie primaire des infections fongiques chez les personnes infectées par le VIH, ce schéma ne figure généralement pas dans les recommandations cliniques actuelles. D'autres études sont nécessaires pour évaluer l'efficacité de schémas autres qu'une prise quotidienne en prophylaxie primaire.
Pour le traitement suppressif ou d'entretien à long terme (prophylaxie secondaire) de la coccidioïdomycose chez les adultes ou adolescents infectés par le VIH ayant une infection documentée et correctement traitée, une dose de fluconazole de 400 mg une fois par jour est généralement recommandée. Pour le traitement suppressif ou d'entretien visant à prévenir la récidive ou la rechute de la cryptococcose chez les adultes ou adolescents infectés par le VIH ayant une infection documentée et correctement traitée, la dose habituelle de fluconazole oral est de 200 mg une fois par jour.
Certains cliniciens recommandent du fluconazole par voie orale à 400 mg par jour pendant les 4 premières semaines, puis 200 mg par jour, comme traitement suppressif à long terme contre la cryptococcose. Si le fluconazole oral est utilisé comme traitement suppressif ou d'entretien à long terme (prophylaxie secondaire) pour prévenir la récidive ou la rechute d'une candidose mucocutanée (oropharyngée, vaginale, œsophagienne) chez des adultes ou adolescents infectés par le VIH présentant des épisodes fréquents ou sévères de ces infections, une dose de 100 à 200 mg une fois par jour est généralement recommandée.
Bien que le fluconazole ait été utilisé à une dose de 200 mg une fois par semaine comme traitement suppressif à long terme chez des femmes infectées par le VIH ayant des antécédents de candidose oropharyngée ou vaginale, ce schéma ne figure généralement pas dans les recommandations cliniques actuelles. Des inquiétudes subsistent quant au fait que cette approche puisse favoriser l'émergence de souches de Candida résistantes au fluconazole. Le traitement suppressif ou d'entretien à long terme pour prévenir la récidive ou la rechute d'infections fongiques chez les patients infectés par le VIH est généralement poursuivi à vie. Cependant, il peut être raisonnable d'interrompre le traitement suppressif ou d'entretien de la cryptococcose chez certains adultes et adolescents ayant obtenu une récupération immunitaire grâce à un traitement antirétroviral combiné efficace.
Prévention des infections fongiques chez les patients transplantés et les patients atteints de cancer
Pour prévenir la candidose chez les receveurs de greffe de moelle osseuse, la dose recommandée de fluconazole est de 400 mg une fois par jour. Chez les patients chez qui une granulocytopénie sévère (numération des neutrophiles inférieure à 500/mm3) est attendue, le traitement par fluconazole doit être commencé plusieurs jours avant la survenue prévue de la neutropénie. Il doit être poursuivi pendant 7 jours après que la numération des neutrophiles a dépassé 1000/mm3.
Posologie pédiatrique
La dose habituelle de fluconazole chez l'enfant varie de 3 à 12 mg/kg/j une fois par jour ; des doses supérieures à 600 mg par jour ne sont pas recommandées. Le fabricant indique qu'une dose de 3, 6 ou 12 mg/kg/j chez l'enfant équivaut respectivement à 100, 200 ou 400 mg par jour chez l'adulte. Certains enfants plus âgés peuvent avoir une clairance comparable à celle des adultes.
Pour traiter une méningite ou une septicémie causée par des Candida sensibles, des nouveau-nés et des nourrissons âgés de 3 mois ou moins ont reçu du fluconazole à une dose de 5 à 6 mg/kg une fois par jour, administré par voie orale ou en perfusion IV sur 1 heure. Chez certains nouveau-nés et nourrissons atteints de septicémie, une dose de charge initiale de 10 mg/kg a été administrée, suivie de 5 mg/kg une fois par jour. D'après les données pharmacocinétiques disponibles chez les prématurés, le fabricant recommande que les nouveau-nés âgés de 2 semaines ou moins reçoivent la même dose quotidienne que les enfants plus âgés, mais administrée une fois toutes les 72 heures.
Candidose oropharyngée et œsophagienne
Pour traiter une candidose oropharyngée ou œsophagienne, le fabricant recommande chez l'enfant 6 mg/kg de fluconazole le premier jour, suivis de 3 mg/kg une fois par jour. La dose pour la candidose œsophagienne peut être augmentée jusqu'à 12 mg/kg par jour si nécessaire, selon l'état du patient et sa réponse au traitement. Le traitement de la candidose oropharyngée doit être poursuivi pendant au moins 2 semaines afin de réduire le risque de rechute. Le traitement de la candidose œsophagienne doit être poursuivi pendant au moins 3 semaines et au moins 2 semaines après la disparition des symptômes.
Autres infections fongiques
Le fluconazole a été administré à une dose de 6 à 12 mg/kg par jour pour traiter les infections candidales systémiques chez l'enfant. Le fabricant recommande de traiter la méningite cryptococcique chez l'enfant par une dose initiale de 12 mg/kg le premier jour, suivie de 6 mg/kg une fois par jour. Si nécessaire, la dose peut être augmentée à 12 mg/kg par jour selon l'état du patient et sa réponse au traitement. Le fluconazole doit être poursuivi pendant 10 à 12 semaines après négativation de la culture du LCR.
Prévention des infections fongiques chez les personnes infectées par le VIH
La dose recommandée de fluconazole oral pour la prophylaxie primaire contre la cryptococcose chez les nourrissons et enfants infectés par le VIH avec une immunodépression sévère est de 3 à 6 mg/kg une fois par jour. Si le fluconazole oral est utilisé comme traitement suppressif ou d'entretien à long terme pour prévenir la récidive ou la rechute d'une cryptococcose ou d'une candidose mucocutanée (oropharyngée, œsophagienne) chez les nourrissons et enfants infectés par le VIH, la dose recommandée est de 3 à 6 mg/kg une fois par jour. Une dose de 6 mg/kg une fois par jour est recommandée pour prévenir la récidive ou la rechute d'une coccidioïdomycose chez ces patients pédiatriques.
Interactions
En général, les interactions avec le fluconazole sont moins fréquentes qu'avec l'itraconazole ou le kétoconazole. L'utilisation de rifampicine avec le fluconazole réduit les concentrations plasmatiques de fluconazole. L'association d'hydrochlorothiazide et de fluconazole a entraîné des augmentations cliniquement peu importantes des concentrations plasmatiques de fluconazole.
Le fluconazole peut interférer avec le métabolisme de certains autres médicaments, principalement en inhibant les isoenzymes du cytochrome P450 CYP3A4 et CYP2C9. Cela peut expliquer les augmentations rapportées des concentrations plasmatiques de bosentan, ciclosporine, midazolam, névirapine, amitriptyline, nortriptyline, phénytoïne, rifabutine, hypoglycémiants sulfamides et natéglinide, inhibiteurs sélectifs de la cyclo-oxygénase-2 tels que le célécoxib et le parécoxib, tacrolimus, triazolam, warfarine et zidovudine. Le fluconazole peut inhiber la formation d'un métabolite toxique du sulfaméthoxazole. Des augmentations des concentrations de térfénadine après de fortes doses de fluconazole ont été associées à des anomalies de l'ECG.
Un effet similaire peut être attendu avec l'astémizole. Cependant, l'utilisation concomitante de fluconazole avec le cisapride pourrait augmenter les concentrations de cisapride et provoquer la toxicité associée. Cette association doit donc être évitée. L'utilisation de fluconazole avec l'astémizole, le cisapride ou la térfénadine doit être évitée en raison du risque d'arythmies cardiaques. Un cas de syncope a été attribué à une augmentation des concentrations d'amitriptyline lors de l'administration concomitante d'amitriptyline et de fluconazole.
Le fluconazole peut également réduire la clairance de la théophylline. Il a été rapporté que la concentration des stéroïdes contraceptifs pouvait augmenter ou diminuer chez des patients recevant du fluconazole, et l'efficacité des contraceptifs oraux peut être affectée. Pour plus d'informations sur les interactions entre les médicaments métabolisés par le cytochrome P450 CYP3A et les azolés, voir la rubrique Itraconazole.
Fluoroquinolones
La lévofloxacine et le fluconazole peuvent tous deux prolonger l'intervalle QT. L'utilisation simultanée de lévofloxacine intraveineuse et de fluconazole a conduit à un épisode de torsades de pointes chez un patient sous hémodialyse.

Interactions microbiologiques
Un effet antifongique synergique a été observé in vitro entre la terbinafine et le fluconazole contre des souches de Candida albicans.
Résistance
L'émergence de souches de Candida spp. résistantes au fluconazole est devenue de plus en plus préoccupante, en particulier chez les patients immunodéprimés recevant une prophylaxie prolongée par fluconazole. Outre la résistance observée chez Candida albicans, des infections dues à Candida dubliniensis, Candida glabrata et Candida krusei, qui peuvent être moins sensibles au fluconazole que Candida albicans, ont été observées chez ces patients. Une résistance secondaire de Candida glabrata a été rapportée au cours d'un traitement par fluconazole.
La résistance au fluconazole a été rapportée comme plus fréquente que celle au kétoconazole ou à l'itraconazole, ce qui peut être lié à l'usage généralisé du médicament. Une résistance croisée avec d'autres azolés ainsi qu'avec l'amphotéricine B a également été signalée.
Une résistance au fluconazole a également été rapportée chez Cryptococcus neoformans et Histoplasma capsulatum. Une histoplasmose est apparue pendant un traitement par fluconazole chez un patient infecté par le VIH. Un C. neoformans résistant au fluconazole a été isolé chez un patient immunocompétent qui n'avait jamais été exposé aux antifongiques azolés.
Interactions médicamenteuses du Fluconazole
Alfentanil
Dans une étude randomisée, en double aveugle, contrôlée par placebo et en crossover menée chez 9 sujets, le fluconazole 400 mg a réduit de 55 % la clairance de l'alfentanil 20 microgrammes/kg et augmenté les effets subjectifs induits par l'alfentanil.
Amitriptyline
Une interaction entre le fluconazole et l'amitriptyline a été rapportée.
- Un garçon de 12 ans atteint d'un rhabdomyosarcome de la prostate a présenté des épisodes de syncope de façon périodique pendant 7 mois alors qu'il prenait du fluconazole pour une mucite induite par la chimiothérapie. Il avait déjà pris du fluconazole auparavant sans problème, mais recevait aussi une dose stable d'amitriptyline pour des douleurs neuropathiques. Après l'arrêt de l'amitriptyline, il n'a plus présenté d'épisodes. L'effet a été confirmé lors d'une nouvelle administration.
L'administration concomitante de fluconazole augmente probablement l'exposition à l'amitriptyline. Trois cas chez l'adulte ont montré des concentrations plasmatiques d'amitriptyline augmentées en cas d'administration concomitante de fluconazole ; chez une patiente de 57 ans, l'intervalle QT s'est allongé et une torsade de pointes est survenue.
Amphotéricine
Les études in vitro et chez l'animal ont donné des résultats contradictoires concernant un antagonisme potentiel entre les effets du fluconazole et de l'amphotéricine sur les espèces de Candida. Cependant, de grandes études randomisées, en double aveugle, comparant le fluconazole avec ou sans amphotéricine pendant 5 jours chez des patients non neutropéniques atteints de candidémie n'ont montré aucun signe d'antagonisme, mais une élimination plus rapide de l'organisme dans le sang et une tendance à une meilleure évolution chez les patients ayant reçu l'association.
Antiacides
L'absorption du fluconazole après administration orale n'est pas influencée par le pH gastrique ; les antiacides comme le co-magaldrox ne l'affectent donc pas.
Antihistaminiques
L'utilisation concomitante de térfénadine avec le fluconazole peut entraîner des concentrations dangereusement élevées de térfénadine, avec un risque de cardiotoxicité. On soupçonne que cela pourrait aussi se produire avec l'astémizole.
Benzodiazépines
Douze hommes en bonne santé ont été inclus dans une étude randomisée, en double aveugle, en crossover à 4 bras afin d'évaluer l'interaction du fluconazole avec le bromazépam. Ils ont reçu une dose unique orale ou rectale de bromazépam (3 mg) après un prétraitement de 4 jours par fluconazole oral (100 mg/jour) ou placebo. Le fluconazole n'a entraîné aucun changement significatif de la pharmacocinétique ou de la pharmacodynamie du bromazépam, qu'il soit administré par voie orale ou rectale.
Le fluconazole a augmenté les concentrations sanguines de midazolam et de triazolam.
Les effets du fluconazole (dose de charge de 400 mg suivie de 200 mg/jour) sur la cinétique du midazolam ont été étudiés chez 10 adultes sous ventilation mécanique recevant une perfusion stable de midazolam. Les concentrations de midazolam ont été multipliées jusqu'à 4 fois après le début du traitement par fluconazole, ces modifications étant plus marquées chez les patients présentant une insuffisance rénale. Pendant l'étude, le rapport hydroxy-midazolam/midazolam a progressivement diminué. Les auteurs ont conclu que, chez les patients en soins intensifs recevant du fluconazole, une réduction de la dose de midazolam devrait être envisagée en cas d'augmentation de la sédation.
Dans une étude portant sur la pharmacocinétique et la pharmacodynamie du midazolam oral 7,5-15 mg, le passage d'une inhibition du métabolisme par itraconazole 200 mg/jour à une induction par rifampicine 600 mg/jour a entraîné une variation allant jusqu'à 400 fois de la surface sous la courbe (AUC) du midazolam oral.
Bloqueurs des canaux calciques
Le fluconazole a augmenté les effets hypotenseurs de la nifédipine en augmentant ses concentrations plasmatiques chez un patient de 16 ans atteint d'un phéochromocytome malin, traité au long cours pour une hypertension artérielle par nifédipine et recevant du fluconazole pour une septicémie à Candida.
Carbamazépine
Le fluconazole peut provoquer une toxicité liée à la carbamazépine, vraisemblablement par inhibition du CYP3A4.
- Un homme de 33 ans sous traitement stable par carbamazépine (400 mg trois fois par jour) pour un trouble convulsif est devenu stuporeux en raison d'une toxicité liée à la carbamazépine après 3 jours de traitement par fluconazole 150 mg/jour. L'arrêt des 2 médicaments a entraîné une baisse des concentrations de carbamazépine (concentration maximale 25 μg/ml) et un retour à son état mental habituel. Le traitement par carbamazépine a ensuite été repris sans autre effet indésirable.
- Les concentrations sériques de carbamazépine ont augmenté lors de l'administration concomitante de fluconazole (400 mg/jour) chez un homme de 38 ans.
Ciclosporine
Le fluconazole peut augmenter les concentrations de ciclosporine en inhibant le CYP3A4. Certaines études n'ont montré que des effets minimes, voire aucun, mais d'autres ont rapporté des augmentations des concentrations sanguines de ciclosporine avec le fluconazole. Les différences de dose et de durée du traitement par fluconazole pourraient expliquer ces divergences. Par exemple, aucune interaction n'a été observée avec une dose de fluconazole de 100 mg/jour, alors que des doses élevées (400 mg/jour ou plus) augmentaient les concentrations sanguines de ciclosporine et de tacrolimus.
L'interaction entre la ciclosporine et le fluconazole a été évaluée rétrospectivement chez 19 receveurs d'une greffe de rein et de pancréas/rein. Le fluconazole par voie intraveineuse et orale a modifié la concentration sanguine de ciclosporine. Cinq sujets n'ont pas eu d'interaction significative, et 15 en ont eu une. Aucun patient n'a présenté de néphrotoxicité ni de rejet de greffe lié au traitement antifongique.
Les effets de doses élevées de fluconazole sur l'immunosuppression par ciclosporine ont été étudiés chez 6 patients transplantés rénaux dans une étude prospective ouverte en crossover. La fonction rénale de base, l'AUC, la Cmax, la Cmin, la fmax et la clairance de la ciclosporine ont été comparées aux jours 2, 4 et 7 après le début du fluconazole oral à 200 mg/jour. À partir du jour 8, la dose de ciclosporine a été réduite de 50 %, et ces paramètres ont de nouveau été évalués au jour 14. Les résultats sont présentés au tableau 1. En ANOVA pour mesures répétées, seules l'AUC et la Cmax au jour 4 de fluconazole étaient significativement plus élevées qu'au jour 0. Il n'y a pas eu de modification significative de la clairance ni de la fmax de la ciclosporine. Les auteurs ont conclu que les variations de Cmin ne sont peut-être pas assez sensibles pour détecter l'interaction décrite et ont suggéré de surveiller l'AUC vers le jour 4 du traitement afin de guider les ajustements de dose de ciclosporine chez tous les patients prenant concomitamment du fluconazole.
Cimétidine
L'absorption du fluconazole après administration orale n'est pas influencée par le pH gastrique ; la cimétidine n'a donc aucun effet.
Clarithromycine
Les effets du fluconazole et de la clarithromycine sur la pharmacocinétique de la rifabutine et de son métabolite, la 25-O-désacétylrifabutine, ont été étudiés chez 10 patients infectés par le VIH. Les patients ont reçu de la rifabutine à la dose de 300 mg, en association avec du fluconazole à la dose de 200 mg et de la clarithromycine à la dose de 500 mg, selon le schéma étudié. L'AUC plasmatique de la rifabutine a augmenté de 76 % lorsque le fluconazole ou la clarithromycine étaient administrés seuls, et de 152 % lorsque les deux médicaments étaient administrés ensemble. Les auteurs ont conclu que les patients devaient être surveillés quant à l'éventuelle survenue d'effets indésirables liés à la rifabutine lorsque celle-ci est coadministrée avec le fluconazole ou la clarithromycine.
Cyclophosphamide
Le cyclophosphamide est un promédicament métabolisé par les enzymes du CYP450 pour produire des composés alkylants cytotoxiques, et l'importance de ce métabolisme est corrélée à l'efficacité et à la toxicité du traitement. Des études in vitro sur six microsomes hépatiques humains ont montré que l'IC50 du Fluconazole pour réduire la production de 4-hydroxycyclophosphamide était de 9-80 μmol/l.
Une étude rétrospective menée chez 22 enfants atteints de cancer a évalué l'interaction potentielle entre le fluconazole et le cyclophosphamide. Des enfants dont le profil de métabolisme du cyclophosphamide était déjà établi, et ne recevant pas d'autres médicaments connus pour modifier ce métabolisme, ont été sélectionnés ; 9 recevaient du fluconazole et 13 servaient de témoins. La clairance plasmatique était significativement plus faible chez les patients recevant également du fluconazole (2,4 contre 4,2 l/heure/m). On ne sait pas clairement si cette interaction est associée à une diminution de l'efficacité thérapeutique du cyclophosphamide.
Doxorubicine
L'effet du Fluconazole sur la pharmacocinétique plasmatique de la doxorubicine a été étudié dans une étude randomisée en cross-over chez des primates non humains. Le Fluconazole (10 mg/kg/jour) a été administré par voie intraveineuse pendant 4 jours avant la doxorubicine (2,0 mg/kg par voie intraveineuse). Le prétraitement par Fluconazole n'a pas modifié la pharmacocinétique de la doxorubicine, et l'incidence de neutropénie sévère (numération absolue des neutrophiles inférieure à 0,5 x 10^9/L) était plus élevée avec la doxorubicine seule qu'avec l'association doxorubicine et Fluconazole. Le Fluconazole ne semble donc pas contribuer aux effets myélosuppresseurs de la doxorubicine.
Flucytosine
L'utilisation concomitante du Fluconazole et de la flucytosine peut avoir un effet additif. Cette association pourrait être utile dans le traitement de la méningite cryptococcique.
Inhibiteurs de la protéase du VIH
L'interaction pharmacocinétique entre Fluconazole 400 mg une fois par jour et indinavir 1000 mg trois fois par jour a été évaluée dans une étude contrôlée contre placebo, en cross-over, sur 8 jours ; aucune interaction significative n'a été observée.
L'effet du Fluconazole sur la pharmacocinétique à l'état d'équilibre du ritonavir et du saquinavir a été étudié chez des patients infectés par le VIH-1. Ils ont reçu l'inhibiteur de protéase (saquinavir 1200 mg trois fois par jour, n = 5, ou ritonavir 600 mg deux fois par jour) seul au jour 1, puis avec Fluconazole 400 mg au jour 2 et 200 mg aux jours 3-8. L'augmentation médiane de l'AUC du saquinavir était de 50 %, et l'augmentation médiane du Cmax de 56 %. En revanche, le Fluconazole n'a pas modifié la pharmacocinétique du ritonavir.
Méthadone
Une interaction entre le Fluconazole et la méthadone (substrat du CYP3A4, du CYP2C9 et du CYP2C) a été rapportée.
Alors qu'il recevait une dose stable de méthadone, un homme de 60 ans atteint d'un cancer avancé a présenté une dépression respiratoire 2 jours après avoir reçu du Fluconazole par voie intraveineuse pour une candidose buccale réfractaire. La naloxone intraveineuse a corrigé cette dépression respiratoire.
Dans une étude randomisée, en double aveugle, contrôlée par placebo, menée chez 25 patients, Fluconazole 200 mg/jour a augmenté les concentrations de méthadone, mais les patients traités n'ont présenté aucun signe ni symptôme notable de surdosage narcotique.
Oméprazole
L'absorption du Fluconazole après administration orale n'est pas influencée par le pH gastrique ; l'oméprazole n'a donc pas d'effet sur ce point. L'oméprazole est largement métabolisé dans le foie par hydroxylation et sulfoxydation, catalysées principalement par le CYP2C19 et le CYP3A4, respectivement. Le Fluconazole est un inhibiteur compétitif puissant du CYP2C19 et un inhibiteur faible du CYP3A4. L'effet du Fluconazole sur la pharmacocinétique d'une dose orale unique d'oméprazole 20 mg a été évalué après une dose orale unique de Fluconazole 100 mg puis après 4 jours d'administration orale à 100 mg/jour chez 18 volontaires masculins sains. Le Fluconazole a augmenté le Cmax et l'AUC moyens de l'oméprazole et a prolongé sa demi-vie (2,59 contre 0,85 heures).
Contraceptifs oraux
Le fluconazole n'a pas modifié de façon significative la pharmacocinétique de l'éthinylestradiol ou du norgestrel, et les investigateurs ont estimé que ce résultat suggérait qu'un traitement par fluconazole chez une utilisatrice de contraceptifs oraux ne devrait pas augmenter le risque de grossesse. Cependant, l'étude utilisait une dose de 50 mg de fluconazole, et l'expérience avec des doses plus élevées a donné des résultats différents.
Dans une autre étude, le fluconazole a réduit la disponibilité systémique de l'éthinylestradiol contenu dans un contraceptif oral, mais les doses utilisées n'ont pas été rapportées.
Dans une étude ouverte en cross-over menée chez 10 sujets jeunes et sains, le fluconazole à la dose de 150 mg a augmenté les concentrations sériques d'éthinylestradiol.
L'interaction pharmacocinétique potentielle entre Fluconazole 300 mg une fois par semaine et un contraceptif oral contenant de l'éthinylestradiol et de la noréthindrone (Ortho-Novum 7/7/7 ; Ortho-McNeil Pharmaceutical Inc, Raritan, NJ) a été étudiée dans une étude contrôlée contre placebo, en double aveugle, randomisée, en cross-over à deux bras, chez 26 femmes saines âgées de 18 à 36 ans. Lors du premier cycle, elles ne prenaient que le contraceptif oral. Lors du deuxième cycle, elles ont été randomisées pour recevoir contraceptif oral + Fluconazole ou contraceptif oral + placebo. Lors du troisième cycle, elles ont reçu l'autre traitement.
Le Fluconazole a entraîné de petites augmentations, mais significatives, de l'AUCo-24 de l'éthinylestradiol et de la noréthindrone. Les volontaires ayant reçu du Fluconazole n'ont pas présenté d'effets indésirables liés au traitement.
Il semble donc qu'il n'y ait pas de risque d'échec contraceptif lié à l'administration concomitante de fluconazole.
Phénytoïne
L'administration concomitante du Fluconazole et de la phénytoïne a entraîné une nette augmentation des concentrations de phénytoïne.
Rifamycines
L'association de la rifampicine et du Fluconazole a des effets insignifiants.
Statines
Les effets du Fluconazole sur les concentrations plasmatiques de fluvastatine et de pravastatine ont été étudiés dans deux études randomisées, en double aveugle, en cross-over, à deux phases différentes. Des volontaires sains ont reçu du Fluconazole par voie orale (400 mg au jour 1 puis 200 mg les jours suivants) ou un placebo. Au jour 4, ils ont reçu une dose orale unique de fluvastatine 40 mg ou de pravastatine 40 mg.
Le Fluconazole a augmenté l'AUC plasmatique et la demi-vie de la fluvastatine de 80 %, mais n'a pas eu d'effet significatif sur la pharmacocinétique de la pravastatine. Le mécanisme probable du ralentissement de l'élimination de la fluvastatine est l'inhibition du CYP2C9. En revanche, la pravastatine ne semble pas exposée à des interactions avec le Fluconazole ni avec d'autres inhibiteurs du CYP2C9.
L'effet du Fluconazole sur la pharmacocinétique de la rosuvastatine a été étudié dans une étude randomisée, en double aveugle, en cross-over à deux bras, contrôlée contre placebo. Des volontaires masculins sains ont reçu 200 mg/jour de fluconazole ou un placebo correspondant pendant 11 jours ; la rosuvastatine 80 mg a été associée au jour 8. Les concentrations plasmatiques de rosuvastatine, de N-désméthyl rosuvastatine, ainsi que des inhibiteurs actifs et totaux de la HMG-CoA réductase ont été mesurées jusqu'à 96 heures après la dose.
Le Fluconazole a augmenté l'AUC et le Cmax de la rosuvastatine de 14 % et 9 % respectivement. Les données limitées disponibles pour le métabolite N-désméthylé ont montré une baisse du Cmax d'environ 25 %. Le Fluconazole n'a pas modifié la proportion d'inhibiteurs actifs ou totaux de la HMG-CoA réductase circulants attribuable à la rosuvastatine. Le Fluconazole n'a donc entraîné que des modifications mineures de la cinétique de la rosuvastatine, sans signification clinique.
Sulfonylurés
L'administration concomitante du Fluconazole avec le tobutamide a entraîné une augmentation des concentrations de tobutamide.
- Un patient de 56 ans, séropositif pour le VIH, diabétique et traité par gliclazide 160 mg/jour, a développé une hypoglycémie sévère pendant un traitement par cotrimoxazole 480 mg/jour et Fluconazole 200 mg/jour. Les auteurs ont supposé que le Fluconazole avait inhibé le métabolisme du gliclazide via l'inhibition du CYP2C9.
Les effets du Fluconazole et de la fluvoxamine sur la pharmacocinétique et la pharmacodynamie du glimépiride ont été étudiés dans une étude randomisée, en double aveugle, en cross-over chez 12 volontaires sains ayant pris du Fluconazole 200 mg/jour (400 mg par jour), de la fluvoxamine 100 mg/jour ou un placebo une fois par jour pendant 4 jours. Au jour 4, ils ont reçu une dose orale unique de glimépiride 0,5 mg.
Le Fluconazole a porté l'AUC moyenne totale du glimépiride à 238 %, la concentration plasmatique maximale à 151 % des valeurs témoins, et la demi-vie du glimépiride est passée de 2,0 à 3,3 heures. Cela est probablement dû à l'inhibition, par le Fluconazole, de la biotransformation du glimépiride médiée par le CYP2C9. Cependant, le Fluconazole n'a pas entraîné de modification statistiquement significative des effets du glimépiride sur la glycémie.
Tacrolimus
Comme le tacrolimus est métabolisé par le CYP3A4 intestinal et hépatique, les médicaments qui inhibent le CYP3A4 peuvent réduire son métabolisme et augmenter ses concentrations sanguines.
L'effet du Fluconazole sur les concentrations sanguines de tacrolimus a été étudié chez huit patients ayant reçu une greffe de foie, chez qui la prophylaxie par Fluconazole (200 mg/jour) a été arrêtée en raison d'une élévation des transaminases hépatiques, d'une dysfonction rénale ou d'une éosinophilie (n = 1 pour chacun). Les concentrations calculées de tacrolimus ont diminué de 13 à 81 % (médiane 41 %) entre le 4e et le 9e jour après l'arrêt du Fluconazole. Les concentrations sanguines de tacrolimus doivent être surveillées de près et les doses ajustées si nécessaire après l'arrêt du Fluconazole.
L'interaction entre le tacrolimus et le Fluconazole a été évaluée rétrospectivement chez 19 receveurs d'une greffe rein-pancréas ou rénale. Le Fluconazole par voie intraveineuse et orale a modifié la concentration sanguine de tacrolimus. Cinq sujets n'ont pas eu d'interaction significative, et 15 en ont eu une. Aucun patient n'a présenté de néphrotoxicité ni de rejet de greffe lié au traitement antifongique.
- Un homme de 17 ans atteint de mucoviscidose, traité par itraconazole après une greffe pulmonaire et hépatique, présentait des concentrations résiduelles élevées de tacrolimus malgré une dose relativement faible (0,1-0,3 mg/kg/jour).
- Un patient prenant tacrolimus 0,085 mg/kg deux fois par jour avec itraconazole 200-400 mg/jour a développé une acidocétose, une neutropénie et une thrombocytopénie, nécessitant l'arrêt des deux médicaments.
- Un receveur de greffe rénale de 34 ans, sous tacrolimus stable et méthylprednisolone, a reçu itraconazole 100 mg deux fois par jour pour une infection urinaire à levures. Le traitement concomitant par Itraconazole a entraîné une augmentation marquée des concentrations résiduelles de tacrolimus dès le deuxième jour (de 13 à 21 μg/ml) ainsi qu'une hausse de la créatinine sérique, nécessitant une réduction de 50 % de la dose de tacrolimus.
Lorsque l'itraconazole a été arrêté, son effet sur la cinétique du tacrolimus a mis 12 jours à disparaître. L'effet inhibiteur de l'itraconazole est apparu rapidement, tandis que sa disparition a été beaucoup plus lente, ce qui est important en pratique clinique. Par conséquent, lors de l'administration concomitante d'itraconazole et de tacrolimus, une surveillance étroite des concentrations sanguines de tacrolimus et des ajustements prudents de la dose sont essentiels pour éviter une toxicité.
Warfarine
La coadministration du Fluconazole et de la warfarine a conduit, dans certains cas, à une prolongation du temps de prothrombine.
Zidovudine
L'association du Fluconazole avec l'acide valproïque a inhibé, in vitro, la glucuronidation de la zidovudine dans des microsomes hépatiques humains plus que d'autres médicaments tels que l'atovaquone et la méthadone.
Effets indésirables
Les effets indésirables rapportés avec le Fluconazole touchent le plus souvent le système gastro-intestinal, notamment douleurs abdominales, diarrhée, flatulences, nausées, vomissements et altération du goût. D'autres effets indésirables comprennent des maux de tête, des vertiges, une leucopénie, une thrombocytopénie, des hyperlipidémies et une élévation des enzymes hépatiques. Une hépatotoxicité grave a été rapportée chez des patients présentant des maladies sous-jacentes sévères comme le SIDA ou un cancer. Des réactions anaphylactiques et des angio-œdèmes ont été rapportés rarement. Les réactions cutanées sont rares, mais des réactions cutanées exfoliatives telles que le syndrome de Lyell (nécrolyse épidermique toxique) et le syndrome de Stevens-Johnson ont été observées, plus souvent chez les patients atteints du SIDA.
Alopécie
Des cas d'alopécie ont parfois été rapportés chez des patients recevant du Fluconazole, en particulier lors d'un traitement prolongé.
Effet sur l'équilibre électrolytique
Une hypokaliémie a été associée au Fluconazole chez 3 patients atteints de leucémie aiguë myéloïde.
Effets sur le cœur
Un allongement de l'intervalle QT et des torsades de pointes ont été rapportés rarement chez des patients recevant du Fluconazole.
Effets sur le foie
Bien que les réactions hépatiques graves liées au Fluconazole soient rares, elles ont été rapportées, en particulier chez des patients présentant des maladies sous-jacentes sévères ou une dysfonction hépatique. Des élévations des enzymes hépatiques sont fréquentes, et des cas d'ictère ont été signalés. Une nécrose hépatique a rarement été observée à l'autopsie chez des patients atteints d'une maladie sévère ayant reçu du Fluconazole. Chez l'un de ces patients, l'hépatotoxicité a été considérée comme dose-dépendante.

Hypersensibilité
Une désensibilisation a été réalisée avec succès chez un patient atteint du SIDA présentant une hypersensibilité au Fluconazole et à l'Itraconazole. Sur sept jours, des doses orales progressivement croissantes de Fluconazole (à partir de 5 mg par jour) ont été administrées ; ensuite, la dose a été maintenue à 400 mg par jour. Aucun effet indésirable n'a été observé pendant la période de désensibilisation ni au cours des trois mois précédant la publication du rapport.
Précautions
Le Fluconazole doit être utilisé avec prudence chez les patients présentant une insuffisance hépatique ou rénale. Des anomalies des bilans hématologiques, hépatiques et rénaux ont été observées chez des patients atteints de maladies sous-jacentes graves telles que le SIDA ou des cancers. Des cas de torsades de pointes et d'allongement de l'intervalle QT ont été rapportés rarement, et la prudence est recommandée lors de l'administration de Fluconazole à des patients présentant des facteurs favorisant les troubles du rythme. Une tératogénicité a été observée chez des animaux recevant des doses élevées de Fluconazole, et son utilisation n'est pas recommandée pendant la grossesse.
Allaitement
Le Fluconazole est excrété dans le lait maternel, à des concentrations similaires à celles du plasma maternel. Cependant, les informations produit ne recommandent pas son utilisation chez les femmes qui allaitent. Dans un rapport, aucun effet indésirable, en dehors d'une légère augmentation du taux de lactate déshydrogénase, n'a été observé chez un nourrisson exposé au Fluconazole par le lait maternel pendant six semaines. En France, le fluconazole est généralement considéré comme compatible avec l'allaitement dans des circonstances cliniques appropriées.
Grossesse
Des doses élevées (toxiques) de Fluconazole, d'Itraconazole et de kétoconazole ont été rapportées comme tératogènes chez les rongeurs.
Bien qu'il existe peu d'informations sur l'utilisation de ces médicaments pendant la grossesse chez l'humain, un cas a été rapporté chez une femme ayant pris du Fluconazole 400 mg par jour pendant toute sa grossesse et ayant donné naissance à un nourrisson présentant de graves anomalies craniofaciales et des membres. Les anomalies ressemblaient à celles associées au syndrome d'Antley-Bixler, une maladie génétique. Néanmoins, un effet tératogène ne pouvait pas être exclu.
Bien que des études de pharmacovigilance n'aient pas mis en évidence d'effets délétères sur le fœtus, des anomalies congénitales ont été observées chez des nourrissons dont les mères avaient reçu de fortes doses de Fluconazole pendant 3 mois ou plus. Les données recueillies par le fabricant concernant 198 femmes exposées à l'itraconazole durant le premier trimestre ont indiqué que le taux de malformations chez les femmes exposées et chez les témoins correspondait au risque de base attendu dans la population générale.
Néanmoins, les fabricants recommandent d'éviter le Fluconazole, l'Itraconazole et le kétoconazole pendant la grossesse. Les informations produit indiquent que des doses de voriconazole équivalentes à celles utilisées en thérapeutique sont tératogènes et embryotoxiques chez les rongeurs. Par conséquent, il est recommandé d'éviter le voriconazole pendant la grossesse et que les femmes en âge de procréer utilisent une contraception efficace pendant le traitement.
Des recommandations similaires ont été formulées pour le posaconazole. D'autres antifongiques azolés, notamment le butoconazole, le clotrimazole, l'éconazole, le miconazole, le sulconazole, la terconazole et le tioconazole, ont été rapportés comme embryotoxiques, mais non tératogènes, chez les rongeurs à fortes doses. Bon nombre de ces médicaments sont utilisés par voie topique ou intravaginale, et l'absorption systémique par ces voies est variable. Bien que ces médicaments ne soient pas nécessairement contre-indiqués pendant la grossesse, il convient de prendre en compte ces risques potentiels lors du choix d'un traitement antifongique chez ces patientes.














